+7 (929) 727 53 60 Травматология / Ортопедия
Оценка влияния остео-пластических материалов на регенерацию костной ткани после операции цистэктомии с резекцией апекса корня
А. В. Капишников*, д.м.н., зав. кафедрой; А. Ю. Розенбаум**, соискатель; В.П. Тлустенко**, д.м.н., профессор, зав. кафедрой; Л.Т. Волова***, д.м.н., профессор, директор; М.А. Постников****, к.м.н., ассистент
- В настоящее время зубосохраняющие операции не теряют свою актуальность в стоматологии.
- Для достижения желаемого результата используют остеопластические материалы, позволяющие ускорить процесс регенерации в зоне дефекта.
- Существует большой выбор костнопластических материалов.
- Также проведено огромное количество исследований эффективности этих материалов.
- Однако, в литературе встречаются противоречивые данные о них.
- С помощью компьютерной томографии были получены данные о плотности костной ткани в зоне операции цистэктомии с одномоментной резекцией верхушки корня зуба с применением деминерализованной спонгиозы «Лиопласт» ® и материала «CrossBone»®.
Ключевые слова: апикальный периодонтит, радикулярная киста, операция резекции верхушки корня зуба, остеопластические материалы, плотность костной ткани, компьютерная томография.
- Currently tooth-saving operations do not lose their relevance in dentistry.
- To achieve the desired result osteoplastic material are used to speed up the process of regeneration in the area of the bone’s defect.
- There is a wide choice of osteoplastic materials. It is also a huge amount of research on the effectiveness of these materials.
- However, in the literature there are conflicting reports about them.
- With the help of computer tomography were obtained data on bone density in the area of operation cystectomy with simultaneous radiectomy using demineralized spongiosis "Lioplast» ® and material «CrossBone» ®.
Keywords: apical periodotitis, radicular cyst, operation of resection of root apex of tooth, osteoplastic materials, bone density, computed tomography.
- Заболевания периодонта занимают третье место по обращаемости к врачу-стоматологу, несмотря на применение современных и высокотехнологичных методов в стоматологии [4].
- Неэффективность терапевтического лечения хронического апикального периодонтита обуславливает применение операции цистэктомии с одномоментной резекцией верхушки корня зуба [10]. После данной операции в костной ткани челюсти остаются полости, которые могут привести к ее деформации.
- Таким образом, реконструкция утраченной костной ткани остается одной из актуальных проблем в стоматологии.
- В настоящее время для улучшения эффективности лечения при зубосохраняющих операциях используют остеопластические материалы[1, 3].
- Такие материалы должны быть биосовместимыми, обладать остеоиндуктивными, а также остекондуктивными свойствами.
- Существует большой выбор остеопластических материалов различных по составу и происхождению, используемых в стоматологии.
- Проведено значительное количество исследований остеопластических материалов с целью выявления наилучших из них [2, 6, 12].
- Все материалы проходят испытания на цитотоксичность путем проведения экспериментов на животных, либо на культуре клеток [7, 8].
- Однако с помощью данных методов затруднительно прогнозировать остеогенез костной ткани и следовательно, судить об эффективности клинического применения того или иного материала, в том числе биогенной деминерализованной спонгиозы «Лиопласт»® и синтетического материала «CrossBone» ®.
- Наиболее достоверным методом исследования клинических результатов применения остеопластических материалов в стоматологии является компьютерная томография (КТ), которая позволяет объективно оценить процессы формирования, плотность и строение регенерата с использованием реперной зоны костной ткани челюсти [5, 9].
Оценить клиническую эффективность применения биогенной деминерализованной спонгиозы «Лиопласт»®и синтетическиого материала «CrossBone»® с помощью компьютерной томографии после цистэктомии с одномоментной резекцией верхушки корня зуба.
- С 2012 по 2014 гг. проводилось лечение 46 пациентов в возрасте 18 - 55 лет.
- Пациенты были разделены на группы: I группа - с диагнозом «хронический апикальный периодонтит» (27 человек) и II группа – диагноз «корневая киста» (19 человек).
- Обработка корневого канала проводилась с использованием сочетания 2 методик StepBack и Crown-Down, с помощью ручных К-, Н- файлов Pro-Endo (VDW, Германия) от 15 до 25 размера по ISO.
- Затем продолжали механическую обработку корневого канала никель-титановыми вращающимися инструментами ProTaper SX, S1, S2, F1, F2 (Dentsply, США).
- С помощью эндодонтического шприца (3 мл) корневой канал ирригировали 0,05% раствором хлоргексидина.
- Затем канал высушивали бумажными пинами.
- Последующую обработку корневого канала осуществляли лазером Waterlase на режиме 1,5 Вт, вода 25%, воздух 35%.
- При обработке корневых каналов длину световода устанавливали меньше измеренной рабочей длины канала на 1,2 мм.
- На лазерном световоде делали отметку перманентным маркером, соответствующую глубине погружения.
- Вводили световод в канал, активировали лазер, и, держа его под углом к противоположной стенке, выводили из канала в течение 10 сек.
- Выключали лазер на выходе из устья канала. Процедуру проводили 3 раза, каждый раз изменяя направление воздействия.
- 23 пациентам первой группы и 11 пациентам II группы в первое посещение в корневой канал закладывали Metapex (MetaBiomed, Южная Корея); 3 и 5 пациентам Iи II группы соответственно данную манипуляцию проводили во второе посещение из-за гнойного отделяемого из корневого канала.
- У трех пациентов из II группы зуб был удален по причине отсутствия положительной динамики.
- Перед цистэктомией всем пациентам пломбировали корневой канал по методу латеральной конденсации гуттаперчевыми штифтами Protaper (Dentsply, США) и силеромAdseal (MetaBiomed, Южная Корея).
- Далее пациентам проводилась зубосохраняющая операция – цистэктомия с одномоментной резекцией верхушки корня (РВК) зуба с заполнением костной полости остеопластическим материалом.
- 43 пациента были разделены на 2 группы в зависимости от использованного остеопластического материала.
- I группа (22 человека) – в качестве остеопластического материала использовали деминерализованную спонгиозу «Лиопласт»® (Самарский банк тканей, Самара).
- Аллогенная деминерализованная спонгиоза, изготовленная по технологии «Лиопласт»® является биогенной и состоит только из компонентов человеческого организма.
- Всем донорам проводится аутопсия и серологическое исследование крови на сифилис и вирусы гепатитов В и С, ВИЧ.
- В Самарском банке тканей применяется оригинальный алгоритм изготовления биопрепаратов из тканей человека, защищенный патентами РФ.
- На первом этапе процесс получения имплантатов включает специальную ультразвуковую обработку тканей для удаления элементов костного мозга и жира из спонгиозы, проведения первичной стерилизации материала, вирусной инактивации.
- После первичной обработки ткани лиофилизируют, а затем герметично упакованный материал стерилизуют радиационным способом.
- II группа (21 человек) – для заполнения костной полости применяли синтетический материал «CrossBone»® (Biotech, Франция).
- Этот материал является полностью синтетическим и представлен смесью гидроксиапатита (60%) и β–трикальций фосфата (40 %).
- Дентальную компьютерную томографию проводили на аппарате «Kodak 9000D» до операции цистэктомии с одномоментной резекцией верхушки корня зуба; непосредственно после операции; через 3 и 6 месяцев после цистэктомии.
- Режим томографии: напряжение на трубке составляет 60-90 кВт, анодный ток от 2 до 15 мА, частота генератора 140 кГц, фокальное пятно 0,5 мм CEI, общая фильтрация 2,5 мм Al.
- Размер сканируемой области (цилиндр) – 50×37 мм, размер трехмерного элемента изображения (изотропный воксел) 0,76×0,76×0,76 мм.
- Доза облучения пациента при одном исследовании составляет 0,04 мЗв (время сканирования 40-45 секунд).
- Проводилось построение серии аксиальных и апроксимальных срезов в области дефекта костной ткани.
- Динамика плотности костной ткани и оценка ее структуры с помощью гистограмм проводилась с использованием пакета прикладных программ для обработки медицинских изображений «Medical Imaging Interaction Toolkit» (MITK 2015.05) [11].
- На всех сроках наблюдения оценивали плотность костной ткани в единицах шкалы Хаунсфильда (HU) в зоне дефекта (HUд).
- Для индивидуальной оценки остеоинтеграции определяли плотность костной ткани в реперной зоне интереса (HUр), которую выбирали в прилежащем к дефекту участке здоровой костной ткани, и расчитывали относительную величину - соотношение HUд/HUp.
Компьютерная томография установила значительные различия в рентгеновской плотности остеопластических материалов «CrossBone»® и «Лиопласт»®.
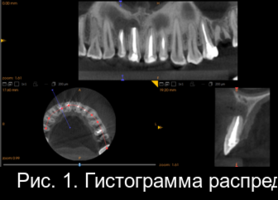
Деминерализованная спонгиоза «Лиопласт»® является рентгенонегативной. Плотность материала, измеренная в первый день после операции РВК (209,08±25,1) оказалась намного меньше плотности здоровой костной ткани (391,25±28,83).
Это объясняется полной декальцинацией этого материала в процессе изготовления и отсутствием в нем минеральных компонентов (рис. 1).
Плотность «CrossBone»® выше плотности костной ткани.
Соотношение плотности зоны дефекта и реперной области (HUд/HUр) на первый день было равно 1,2±0,11.
Высокая плотность «CrossBone»® обусловлена наличием в его составе только неорганических компонентов (рис. 2).
Рис. 1. Гистограмма распределения плотности на дентальной компьютерной томографии фронтального отдела верхней челюсти пациентки О. непосредственно после операции РВК зуба 1.1, 1.2 с заполнением костной полости деминерализованной спонгиозой «Лиопласт»®.
Рис. 2. Гистограмма распределения плотности на дентальной компьютерной томографии фронтального отдела нижней челюсти пациента М. непосредственно после операции РВК зуба 4.1 с заполнением костной полости материалом «CrossBone»®.
Компьютерные томограммы 22 пациентов I группы показали замещение костного дефекта регенерата через 3 месяца после операции: определяется формирующийся трабекулярный рисунок границы костной полости не дифференцируются от окружающих тканей.
Образование новой костной ткани подтверждено результатами измерения плотности костной ткани.
При использовании деминерализованной спонгиозы «Лиопласт»® через 3 месяца уровень поглощения (HU) костной ткани, формирующейся в области дефекта приближается по своему к плотности реперной зоны.
Средний прирост плотности костной ткани у пациентов I группы составил 86% (табл. 1).
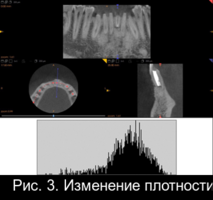
Образование новой костной ткани доказывает соотношение плотности операционной области к здоровой костной ткани, которое в первый день после РВК составляло 0,53±0,04. , а к концу третьего месяца его значение увеличилось практически в 2 раза и приблизилось к единице (рис.3).
Через 6 месяцев все показатели оставались неизменными.
На КТ у 21 пациента II группы на всех сроках наблюдения отчетливо видны гранулы материала, которые не были подвержены резорбции.
Показатели плотности операционной зоны через 3 и 6 месяцев после РВК при применении материала «CrossBone»® схожи с первым днем после операции (рис.3).
Отношение плотности в операционной области к здоровой костной ткани (HUд/HUp) также остается выше 1,0 (табл. 1).
Табл.1. Показатели костной ткани в реперной зоне и в области операции РВК с применением остеопластических материалов «Лиопласт»®, «CrossBone».
Рис. 3. Изменение плотности костной ткани в области дефекта на следующий день после операции РВК, через 3 и 6 месяцев.
Клинический пример №1
Пациентка Т., 35 лет. Обратилась на прием с жалобами на ноющую боль, чувство дискомфорта в области зуба 1.4.
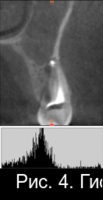
Основываясь на данных клинико-рентгенологического исследования был поставлен диагноз «хронический апикальный периодонтит 1.4» (рис. 4,а).
Пациентке была проведена операция цистэктомии с одномоментной резекцией верхушки корня зуба с последующим заполнением костной полости деминерализованной спонгиозой «Лиопласт»®.
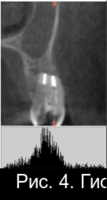
Рис. 4. Гистограммы распределения плотности на дентальной компьютерной томографии правого сегмента верхней челюсти пациентки Т. до операции РВК зуба 1.4 с применением деминерализованной спонгиозы «Лиопласт»®(а); через 3 месяца после операции РВК (б); через 6 месяцев после операции РВК (в).
На рисунках 4(б) и 4(в) отчетливо наблюдается заполнение послеоперационного дефекта костным регенератом.
Границы новообразованной ткани не дифференцируются от окружающих костных структур.
Распределение плотности на гистограмме через 3 месяца после операции смещается к более высокому уровню (рис. 4,б).
Нарастание доли плотного компонента установлено через 3 месяца (рис. 4,б), при этом гетерогенный характер гистограммы свидетельствует о неравномерности формирования костной ткани.
Структура плотности в операционной зоне на шестом месяце наблюдения (рис. 4,в) приобретает гомогенность и находится в диапазоне, характерном для губчатого вещества кости.
Клинический пример № 2
Пациент М, 22 года обратился на прием с жалобами на ноющую боли, чувство распирания в зубе 4.1.
Основываясь на данных рентгенологического исследования был поставлен диагноз «хронический апикальный периодонтит 4.1».
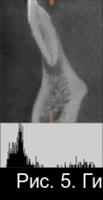
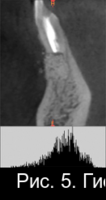
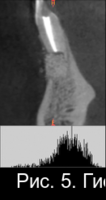
Рис. 5. Гистограммы распределения плотности на дентальной компьютерной томографии фронтального сегмента челюсти пациента М. до операции РВК зуба 4.1 с применением «CrossBone»®(а); через 3 месяца после операции РВК (б); через 6 месяцев после операции РВК (в).
На рисунках 5(б) и 5(в) отчетливо видна костная полость, заполненная гранулами материала «CrossBone»®, который не меняет свою конфигурацию, не резорбируется и не замещается костной тканью на протяжении всего срока наблюдения.
Отчетливая дифференцировка этого материала от губчатого вещества сохраняется и через 6 месяцев после операции.
Анализ серии гистограмм (рис.2, рис.5,б и рис.5,в) в зоне дефекта подтверждает высокую плотность и статичность указанного материала.
- Компьютерная томография позволяет объективно оценить остеоиндуктивный потенциал остеопластических материалов, применяемых в стоматологии.
- Индивидуальная количественная характеристика формирования костной ткани на томограммах может быть получена путем сравнения операционной и реперной зон интереса с построением гистограмм рентгеновской плотности.
- Синтетический материал «CrossBone» является биоинертным, нерезорбируемым остеопластическим материалом не обладающим остеоиндуктивными свойствам.
- Деминерализованная спонгиоза «Лиопласт»® представляет собой биосовместимый остеопластический материал, обеспечивающий формирование костной ткани уже через 3 месяца после операции РВК.
10. Список использованной литературы
- Ешиев А.М., Сагынбаев М.А., Алимжанов С.К. Эффективность остеоцистэктомии с применением остеопластических материалов // Фундаментальные исследования. - 2015. - № 1-3. С. 500-503.
- Eshiev A.M., Sagynbaev M.A., Alimzhanov S.K. EHffektivnost' osteocistehktomii s primeneniem osteoplasticheskih materialov // Fundamental'nye issledovaniya. - 2015. - № 1-3. S. 500-503.
- Кириченко В.Н., Марченко Н.В. Экспериментальное обоснование применения биологических и синтетических остеопластических материалов при хирургическом лечении генерализованного пародонтита // Крымский терапевтический журнал. - 2011.- № 2 (17). С. 66-68.
- Kirichenko V.N., Marchenko N.V. EHksperimental'noe obosnovanie primeneniya biologicheskih i sinteticheskih osteoplasticheskih materialov pri hirurgicheskom lechenii generalizovannogo parodontita // Krymskij terapevticheskij zhurnal. - 2011.- № 2 (17). S. 66-68.
- Модина Т.Н., Маклакова И.С. Опыт использования нового отечественного остеопластического материала при лечении деструктивных форм периодонтита // Эндодонтия Today. - 2012. - № 1. С. 28-30.
- Modina T.N., Maklakova I.S. Opyt ispol'zovaniya novogo otechestvennogo osteoplasticheskogo materiala pri lechenii destruktivnyh form periodontita // EHndodontiya Today. - 2012. - № 1. S. 28-30.
- Петрикас А.Ж., Захарова Е.Л., Ольховская Е.Б. Распространенность осложнений кариеса зубов // Стоматология. – 2014. -№ 1.-С.19-20.
- Petrikas A.ZH., Zaharova E.L., Ol'hovskaya E.B. Rasprostranennost' oslozhnenij kariesa zubov // Stomatologiya. – 2014. -№ 1.-S.19-20.
- Постников, М. А. Использование компьютерной томографии в ортодонтии / Г. В. Степанов, А. Б. Елизаров, А. М. Хамадеева, М. А. Постников // Экран муниципального здравоохранения. – Самара: ООО «Офорт», 2007. – № 9. – С. 35-36.
- Postnikov, M. A. Ispol'zovanie komp'yuternoj tomografii v ortodontii / G. V. Stepanov, A. B. Elizarov, A. M. Hamadeeva, M. A. Postnikov // EHkran municipal'nogo zdravoohraneniya. – Samara: OOO «Ofort», 2007. – № 9. – S. 35-36.
- Федорова М.З., Надеждин С.В., Посохова В.Ф., Чуев В.В., Шатерникова В.А. Оценка биоактивности и биосовместимости остеопластического материала в опытах invitro и invivo. Научные ведомости Белгородского государственного университета. Серия: Медицина. Фармация. - 2012. - Т. 18. № 10-3 (129). С. 124-129.
- Fedorova M.Z., Nadezhdin S.V., Posohova V.F., CHuev V.V., SHaternikova V.A. Ocenka bioaktivnosti i biosovmestimosti osteoplasticheskogo materiala v opytah invitro i invivo. Nauchnye vedomosti Belgorodskogo gosudarstvennogo universiteta. Seriya: Medicina. Farmaciya. - 2012. - T. 18. № 10-3 (129). S. 124-129.
- Anderson J.M., Rodrigues A., Chang D.T. Foreign body reaction to biomaterials // Semin. Immunol. – 2008. – 20(2). – P. 86-100.
- Dee K.C., Rueger D.C., Andersen T.T., Bizios R. Conditions which promote mineralization at the bone-implant interface: a model in vitro study // Biomaterials. - 1996. - Vol. 17, No. 2. - P. 209-215.
- Hao Y1, Zhao W, Wang Y, Yu J, Zou D. Assessments of jaw bone density at implant sites using 3D cone-beam computed tomography // Eur Rev Med Pharmacol Sci. - 2014. - 18(9):1398-1403.
- Livada R, Fine N, Shiloah J. Root amputation: a new look into an old procedure// N Y State Dent J. 2014. Vol. 80. №4. P.24.
- Medical_Imaging_Interaction_Toolkit: [Электронныйресурс] URL: http://mitk.org/wiki/The_Medical_Imaging_Interaction_Toolkit_(MITK).
- Tomsia A.P., Launey M.E., Lee J.S., Mankani M.H., Wegst U.G.K., Saiz E. Nanotechnology Approaches for Better Dental Implants // Int J Oral Maxillofac Implants. – 2011. - 26 (Suppl). – P. 25–49.
-
Эффективность операции коронального смещения с мембраной ТМО «Лиопласт-С»® для лечения множественных рецессий
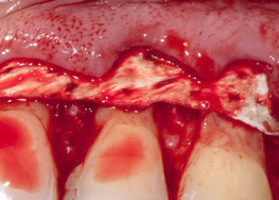 Файл статьи Клинико-экспериментальное исследование. Проведен анализ результатов оперативного лечения у одиннадцати пациентов устранения множественных рецессий десны 1-го и 2-го класса по Miller (1983).
Подробнее
Файл статьи Клинико-экспериментальное исследование. Проведен анализ результатов оперативного лечения у одиннадцати пациентов устранения множественных рецессий десны 1-го и 2-го класса по Miller (1983).
Подробнее
-
Optical analysis of Implants from the Dura Mater. Спек-тральный анализ Раманов-ским методом имплантатов из ТМО (dura mater)
 Файл статьи The results of the spectral analysis using the method of Raman scattering spectroscopy (RS) of dura mater (DM) samples, manufactured by technology “Lyoplast” practised in clinic in multiple gum recessions treatment.
Подробнее
Файл статьи The results of the spectral analysis using the method of Raman scattering spectroscopy (RS) of dura mater (DM) samples, manufactured by technology “Lyoplast” practised in clinic in multiple gum recessions treatment.
Подробнее
-
Применение костных аутотрансплантатов и индивидуальных аллогенных костных блоков при атрофии альвеоляра нижней челюсти
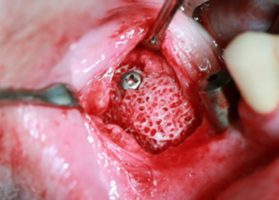 Файл статьи Клинико-экспериментальное исследование. Применение индивидуальных костных аллоблоков для реконструкции челюстей. Отработка хирургической методики. Сравнение с аутоблоками.
Подробнее
Файл статьи Клинико-экспериментальное исследование. Применение индивидуальных костных аллоблоков для реконструкции челюстей. Отработка хирургической методики. Сравнение с аутоблоками.
Подробнее
-
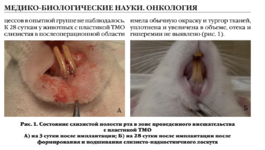
Создание экспериментальной модели in vivo для изучения хирургической техники в двуслойной методике лечения множественных рецессий
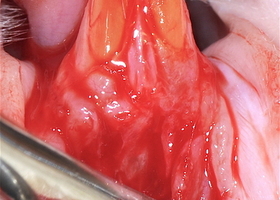 Файл статьи Лабораторное исследование на животных. Использование аутотрансплантата и мембраны ТМО (dura mater) для лечения множественных рецессий десны. Сравнительный анализ результата.
Подробнее
Файл статьи Лабораторное исследование на животных. Использование аутотрансплантата и мембраны ТМО (dura mater) для лечения множественных рецессий десны. Сравнительный анализ результата.
Подробнее