+7 (929) 727 53 60 Травматология / Ортопедия
Создание экспериментальной модели in vivo для изучения хирургической техники в двуслойной методике лечения множественных рецессий
УДК 616.311.2-06-092.9-089.844-74
СОЗДАНИЕ ЭКСПЕРИМЕНТАЛЬНОЙ МОДЕЛИ IN VIVO АДЕКВАТНОЙ ХИРУРГИЧЕСКОЙ ТЕХНИКЕ В ДВУХСЛОЙНОЙ МЕТОДИКЕ ЛЕЧЕНИЯ МНОЖЕСТВЕННЫХ РЕЦЕССИЙ ДЕСНЫ С ПРИМЕНЕНИЕМ ПЛАСТИЧЕСКОГО МАТЕРИАЛА
М.А. НОСОВА
Самарский государственный медицинский университет
Разработана экспериментальная модель in vivo адекватная техника коронального смещения в двухслойной методике для лечения множественных рецессий десны с применением пластического материала.
Воспроизведено хирургическое вмешательство на нижней челюсти крыс с оценкой взаимодействия оперируемых тканей с пластическим материалом.
В данном исследовании использован пластический материал аллогенного происхождения — ТМО (твердая мозговая оболочка).
Наблюдения за животными проводились на протяжении 28 дней, результаты оценивали по стоматологическому статусу и макроскопическим препаратам.
В эксперименте показана эффективность применения аллогенной ТМО.
Предложенная хирургическая модель является универсальной для оценки взаимодействия тканей с любым пластическим материалом.
Ключевые слова: Экспериментальная модель, пластический материал, ТМО — твердая мозговая оболочка, множественные рецессии, двухслойная техника.
Носова Мария Александровна, соискатель института экспериментальной медицины и биотехнологий СамГМУ, 5115895@rambler.ru.
CREATION OF EXPERIMENTAL MODEL IN VIVO TO ADEQUATE SURGICAL TECHNIQUE IN DOUBLE-LAYER METHODOLOGY OF TREATMENT OF MULTIPLE GUM RECESSIONS WITH THE USE OF PLASTIC MATERIAL
М.А. Nosova,
Institute of Experimental medicine and Biotechnology of SamSMU
An experimental model in vivo adequate to the technique of coronal bias in a two-layer technique for treating multiple gum recessions with the use of plastic material was developed.
Reproduced surgical intervention on the lower jaw of rats, with an assessment of the interaction of operated tissues with plastic material. In this study, plastic material of allogeneic origin (dura mater) was used.
Observations of the animals were carried out for 28 days, the results were evaluated for dental status and macroscopic drugs.
In the experiment, the effectiveness of allogeneic TMO is shown.
The proposed surgical model is universal for evaluating the interaction of tissues with any plastic material.
Key words: Experimental model, plastic material, TMO-solid dura mater, multiple recessions, two-layer technique.
Nosova Maria Aleksandrovna, competitor of Institute of Experimental medicine and Biotechnology SamSMU, 5115895@rambler.ru.
В настоящее время рецессия десны является одним из ведущих клинических признаков патологии пародонта. Известные в литературе понятия рецессии десны, представляющие собой прогрессирующее смещение десны в направлении верхушки корня зуба, причиной которого является атрофия всех окружающих зуб тканей. Рецессии десны бывают одиночные и множественные (в области 3-х и более рядом расположенных зубов) [13]. Множественные рецессии десны встречаются в 71,4% случаев [5]. К множественным поражением слизистой десны могут приводить врожденные и приобретенные факторы. Такая утрата тканей пародонта приводит не только к развитию гиперчувствительности зубов, но и к эстетическим дефектам, а также к некариозным поражениям твердых тканей зубов, и, как следствие, к полной потере зуба [14]. Именно поэтому хирургические вмешательства по устранению рецессий десны занимают одно из важных мест в ряду зубосохраняющих операций.
Для лечения множественных рецессий десны на сегодня приоритетной и наиболее прогностической является операция коронально-смещенного ротированного слизисто-надкостничного лоскута предложенная M de Sanctis и G. Zuссhelli в 2000-ом году [16]. В большинстве клинических случаев (более 87.3%) этот метод требует применение пластического материала.
Золотым стандартом среди пластических материалов является аутотрансплантат [9]. Забор аутотрансплантата для этих целей проводят в области твердого неба. В результате создается второе операционное поле, что влечет за собой все очевидные недостатки и, как следствия, - послеоперационные осложнения на ранних и отдаленных сроках, а также, приводит к увеличению времени операции и рискам рецидивов в 17.2% случаев [7,8]. Кроме того, размер донорской зоны не позволяет провести операцию у пациентов с рецессиями десны в области 3-х и более зубов, а в 20% случаев забор аутотрансплантата становится невозможным, по причине конституциональных особенностей и атрофических процессов у пациента [6,10].
Перечисленные недостатки и ограничение объема аутотрансплантата, вызвали необходимость поиска альтернативных пластических материалов. За последние 20 лет было предложено множество различных материалов, преимущественно биогенной природы (ксеногенные, аллогенные и комбинированные) [15]. Очевидно, что эффективность любой медицинской технологии и изделий медицинского назначения, во многом обусловлена полноценным проведением доклинических испытаний с использованием адекватных экспериментальных моделей [11,3] индекс 8,7.
На сегодня существуют несколько экспериментальных моделей, созданных для изучения, либо самой хирургической техники, либо свойств пластического материала. Например, использование в качестве пластического материала отечественного композиционного продукта, состоящего из аутологичных мезенхимальных клеток из жировой ткани, костного коллагена и гидроксиапатита. В эксперименте препарат помещали на смоделированную рецессию десны у кроликов и оставляли для заживления вторичным натяжением, оценивая результат по различным показателям в динамике [2]. Так же известны исследования по доклиническим испытаниям с применением препаратов ксеногенного происхождения. Коллагеновая матрица Mucograft была имплантирована экспериментальным животным без перекрытия слизистой, предполагающее заживление раневой поверхности вторичным натяжением [1]. Явным недостатком этих экспериментальных моделей, является заживление операционной раны вторичным натяжением, и как следствие, контакт пластического материала с полостью рта и ротовой жидкостью. Чтобы исключить эти недостатки, в качестве прототипа взята операция коронально-ротированного лоскута Zucchelli, применяемая для лечения множественных рецессий в клинике, в которой пластический материал полностью перекрывается слизисто-надкостичным лоскутом, заживление происходит первичным натяжением, и пластический материал не контактирует с ротовой полостью [12]. В этой операции в качестве пластического материала нами впервые предложено использовать аллогенную лиофилизированную твердую мозговую оболочку (заявка на патент). Для обоснования клинического применения ТМО, было необходимо провести доклинические исследования на животных.
Поэтому целью нашей работы явилась разработка экспериментальной модели in vivo адекватной хирургической технике в двуслойной методике лечения мно жественных рецессий десны с применением пластического материала.
При разработке экспериментальной модели использованы: крысы стока Wistar категории II (n= 32) обоего пола. Животные содержались в условиях вивария, при свободном доступе к корму и воде. Все манипуляции с лабораторными животными выполнялись в соответствии с «Европейской конвенцией защиты позвоночных животных, используемых в экспериментальных и других научных целях», а также в соответствие с ГОСТ Р 53434-2014 «Принципы надлежащей лабораторной практики».
В ходе проведения исследования и выполнения экспериментальных моделей все животные были разделены на 2 группы:
Группа контроля без пластики (n=16) – крысам проводили экспериментальную операцию, адекватную двуслойной технике устранения рецессий слизистой десны по Zucchelli;
Группа опытная (n=16) – крысам проводили экспериментальную операцию, адекватную двуслойной технике устранения рецессий слизистой десны по Zuccelli с применением пластического материала – твердой мозговой оболочки.
Зондировании тканей пародонта и пальпации операционной области. Наличие или отсутствие отека мягких тканей снаружи, отека, гиперемии, цианотичности тканей пародонта. Глубина зондирования зубодесневой борозды (измерение градуированным зондом в мм). Диагносцировали подвижность оперируемых зубов.
Способ получения аллогенного имплантата из ТМО крыс.
В процессе создания биоимплантов из твердой мозговой оболочки крыс проводится в соответствие с алгоритмом производства биоимплантатов «Лиопласт»® из соединительных и опорных тканей человека для клинических целей, проводится ультразвуковая обработка тканей с последующей их лиофилизацией, а затем герметично упакованный материал стерилизуют радиационным методом [4]. Проводится комплексный контроль качества готового материала. Применение химических факторов при изготовлении биоимплантатов применяются в минимальном количестве для сохранения структуры и биохимического компонента материала.
Наблюдения за животными проводились в динамике в течение 28 суток. Оценивали состояние животных в послеоперационном периоде и их стоматологический статус. Параметры оценки были основаны на визуальном осмотре. Обращали внимание на наличие или отсутствие отека мягких тканей, гиперемии и цианотичности слизистой в области операции. Проводили зондировании тканей пародонта и пальпацию операционной области. Измерение глубины зубодесневой борозды осуществляли градуированным зондом. Диагносцировали подвижность оперируемых зубов.
У всех животных поле эвтаназии оценивали состояние слизистой в зоне выполненной операции, отмечали цвет слизистой, наличие/отсутствие признаков воспаления и прочих осложнений со стороны зубо-челюстной системы. Макрообъекты, представленные 2 нижними резцами и фрагментом нижней челюсти выделяли острым путем (режущим инструментом – пила).
Экспериментальное моделирование пластических операций коронально смещенным лоскутом адекватно операции Zucchelli на крысах
За 24 ч. до предполагаемой операции у животных убирали корм, при сохранении свободного доступа к воде. Все операции выполняли с использованием комбинированной анестезии (золетил 30 мг/кг +рометар 20 мг/кг).
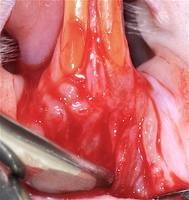
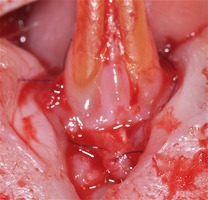
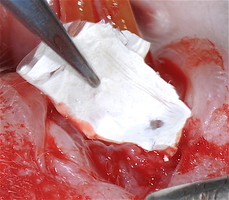
Перед операцией у животных удаляли шерсть в области преддверия рта. Животных размещали в положении на спине. Вмешательство выполняли в проекции двух нижних резцов. Для этого проводили обработку слизистой в области вмешательства раствором хлоргексидина 0,05%. На вестибулярной поверхности слизистой выполняли поперечный разрез слизистой в пределах двух нижних резцов. Затем продольно, двигаясь по направлению к корням нижних резцов, формировали слизисто-надкостничный лоскут с помощью двустороннего микрохирургического скальпеля (Micro-Blade Hu-Friedy), который мобилизовывали. Предварительно выкроенную по размеру лоскута и предварительно регидратированную в изотоническом растворе до 5 минут ТМО укладывали с одной стороны на шейки зубов с другой - на переднюю поверхность нижней челюсти и прикрывали слизисто-надкостничным лоскутом, который фиксировали отдельными узловыми, а также кисетным швом нитями пролен 6/0 к слизистой в проекции шеек двух нижних резцов крысы.
В послеоперационном периоде животных ежедневно осматривал ветеринар. Основной зоной интереса было состояние наложенных швов и выраженность отека слизистой полости рта. При выявлении признаков, свидетельствующих о наличии боли и дискомфорта в области раны проводили инъекции обезболивающих препаратов (анальгин, ксефокам). После проведения вмешательств на зубо-челюстной системе животным скармливали стандартный, предварительно размягченный корм в течение 7 суток. По истечении контрольных сроков: 3, 7, 14, 28 проводили эвтаназию путем введения в наркоз (золетил 30 мг/кг + рометар 20 мг/кг) с последующим введением внутрисердечно летальной дозы тиопентала натрия.
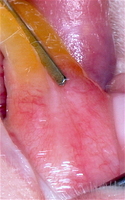
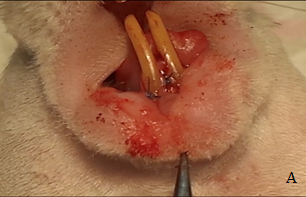
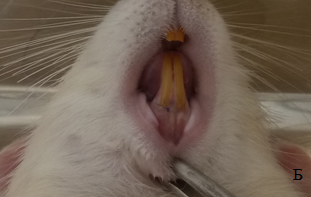
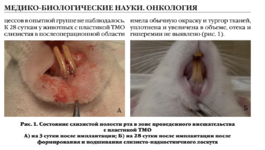
Визуальный осмотр и макроскопическое исследование зубочелюстной области крыс в контрольные сроки на 3, 7, 14, 28 сутки показали, что в зоне проведенного вмешательства слизистая сохраняет свой цвет и консистенцию. На 3 сутки швы состоятельны, отделяемого нет, признаков воспаления не обнаружено. Видимый отек слизистой нижней челюсти у всех животных опытной серии достигал максимума на 4-5 сутки, а к 7-8 суткам разрешался полностью. Такая же динамика течения раневого процесса была в группе контроля. Кроме того, у животных этой группы отмечено формирование глубоких парадонтальных карманов и подвижность двух нижних резцов в проекции которых выполнено оперативное вмешательство. Подобных патологических процессов в опытной группе не наблюдалась. К 28 суткам у животных с пластикой ТМО, слизистая в послеоперационной области имела обычную окраску и тургор тканей, уплотнена и увеличена в объеме, отека и гиперемии не выявлено (рис 1).
Рисунок 1. Состояние слизистой полости рта в зоне проведенного вмешательства с пластикой ТМО
А) на 3 сутки после имплантации; Б) на 28 сутки после имплантации после формирования и подшивания слизисто-надкостничного лоскута
Таким образом, создана экспериментальная хирургическая модель в области слизистой передних резцов нижней челюсти крыс, аналогичная двуслойному методу лечения множественных рецессий десны у пациентов по Zuccelli с использованием пластического материала.
В эксперименте применение аллогенной лиофилизированной ТМО в этой операции продемонстрировала безопасность и эффективность использованного пластического материала.
Данная экспериментальная хирургическая модель может быть использована для оценки взаимодействия тканей реципиента с любым пластическим материалом.
- Баулин И.М. Экспериментально-клиническое обоснование применения коллагеновой матрицы для увеличения объема десны: Дисс. ... канд. мед. наук. — М., 2015. — 126 с.
- Баулин И. М., Бадалян В. А., Ряховский А. Н., Экспериментальное исследование коллагеновой матрицы для увеличения объема десны с использованием 3D-моделирования. Центральный научно-исследовательский институт стоматологии и челюстно-лицевой хирургии Минздрава России, Москва, Россия). DOI:10.17116/stomat20159458-10, Журнал: Стоматология. 2015;94(5): 8-10
- Волова Л.Т. Биологическая система оценки качества биоимплантатов с помощью клеточных технологий, Успехи современного естествознания. 2008. № 5. С. 70-71.
- Волова Л.Т. Способ изготовления крупноблочных лиофилизированных костных имплантатов. патент на изобретение RUS 2366173 15.05.2008.
- Вольф Герберт Ф., Ратейцхак Эдит М, Ратейцхак Клаус. Парадонтология. 2008. – 548с.
- Григорянц Л.А., Ганжа И.Р. Роль пластической пародонтальной хирургии при увеличении прикрепленной десны для устранения локальной и генерализованной рецессии // Клиническая стоматология. – 2006. – №2. – C. 35-40. 40.
- Грудянов А.И., Ерохин А.И. Хирургические методы лечения заболеваний пародонта. - М.: Медицинское информационное агентство, 2006. – 127 с. 21.
-
Доклад на IV Международной научно-практической конференции «Современная гнатология»
 Файл анонса
М.А. Носова, Д.Д. Березина, Л.Т. Волова, А.Н. Шаров, Д.А. Трунин, М.А. Постников
Подробнее
Файл анонса
М.А. Носова, Д.Д. Березина, Л.Т. Волова, А.Н. Шаров, Д.А. Трунин, М.А. Постников
Подробнее
-
Морфологическое и лабора-торное обоснование приме-нения комбинированных трансплантатов при костной пластике челюстей
 Экспериментальное исследование. Изучение морфогенеза после заме-щения дефектов нижней челюсти смесью лиофилизированной алло-спонгиозы и “аллогенного гидроксиапатита” в соотношении 1:1 и 3:1.
Подробнее
Экспериментальное исследование. Изучение морфогенеза после заме-щения дефектов нижней челюсти смесью лиофилизированной алло-спонгиозы и “аллогенного гидроксиапатита” в соотношении 1:1 и 3:1.
Подробнее
-
Эффективность применения биоимплантатов на основе аллогенной деминера-лизованной спонгиозы в детской стоматологии
 Эффективность применения биоимплантатов "Лиопласт-С"® на основе аллогенной деминерализованной спонгиозы при замещении дефектов после удаления одонтогенных кист в у детей
Подробнее
Эффективность применения биоимплантатов "Лиопласт-С"® на основе аллогенной деминерализованной спонгиозы при замещении дефектов после удаления одонтогенных кист в у детей
Подробнее
-
Восстановление структуры кости с помощью аллогенного гидроксиапатита Лиопласт у животных с эксперимен-тальной остеорезорбцией
 Лабораторное исследование. Иньекционный способ введения аллогенного гидроксиапатита полученного при деминерализации костных биоимплантатов для восстановления костной ткани.
Подробнее
Лабораторное исследование. Иньекционный способ введения аллогенного гидроксиапатита полученного при деминерализации костных биоимплантатов для восстановления костной ткани.
Подробнее