+7 (929) 727 53 60 Травматология / Ортопедия
ДОКУМЕНТЫ И ЛИЦЕНЗИИ
Применение биоимплантатов "Лиопласт"® одобрено Министерством здравоохранения.
ТУ-9398-001-01963143-2004 Регистрационное удостоверение ФС 01032004/1567-05 от 29 апреля 2005 года.
Забор донорского материала производится в соответствии с Законом Российской Федерации «О трансплантации органов и тканей» №4181-1 от 22.11.1992 г.
Лицензия РФ М99-01 -0021 04 от 9 февраля 2006 г.
Требование к использованию, транспортировке и хранению:
- Биомплантаты транспортируются всеми видами крытых транспортных средств в соответствии с правилами перевозки грузов, действующими на соответствующем виде транспорта.
- Вид отправки: почтовой посылкой и всеми видами транспорта (автомобильным, авиа и железнодорожным) по ГОСТ 20435 или ГОСТ 18477.
- Условия транспортирования биоимплантатов – по условиям хранения 5 (ОЖ4) ГОСТ 15150.
- Биомплантаты в упаковке предприятия изготовителя должны храниться в условиях хранения 1 ГОСТ 15150. при температуре от +1°С до+30ºС.
- Каждый биоимплантат должен быть уложен в индивидуальную двойную упаковку пленка-пленка, пленка-бумага, производства "Wiburiy oy wipak medical", Финляндия, Бакстер, или в стеклянные флаконы объемом от 5 до 100 мл.
- Упаковка пленка-пленка, пленка бумага должны быть герметично заварены с маркировкой упаковки пленка-пленка индикатором гамма стерилизации (Цветовые индикаторы выбираются согласно ГОСТ Р 50325-92).
- Материал, упакованный в стеклянные флаконы должен быть герметично закрыт резиновой пробкой и алюминиевым колпачком (ГОСТ Р ИСО 10993, ОСТ 64-2-82-85, ГОСТ Р 51314-99).
- Индивидуальные упаковки с биоимплантатами должны быть уложены в количестве от 1-го до 5-ти в коробку из картона ГОСТ 9142, ГОСТ 9481, ГОСТ 13511, ГОСТ 13512,. ГОСТ 13513, ГОСТ 13516, ГОСТ 13841.
- После вскрытия упаковки, биоимплантат должен быть использован, а неиспользованный материал – утилизирован.
- Транспортную тару с биоимплантатами оклеивают лентой полиэтиленовой с липким слоем ГОСТ 20477 или лентой клеевой на бумажной основе ГОСТ 18251 или бумагой ГОСТ 10459.
Комплект поставки:
- биоимплантаты -1 шт.
- потребительская упаковка -1 шт.
- этикетка - 1 шт.
- инструкция по применению -1 шт. на групповую упаковку.
2. Предварительные анализы и тесты материала и потенциальных доноров
Биоимплантаты полученные по технологии «Лиопласт» состоят только из компонентов человеческого организма, не содержат внесенных извне химических веществ.
Всем донорам проводиться аутопсия и серологическое исследование крови на сифилис и вирусы гепатитов В и С, СПИД.
Технология производства биоимплантатов «ЛИОПЛАСТ» позволяют полностью защитить реципиента от передачи ему какого-либо заболевания, сводят до минимума опасность инфицирования персонала и делают процесс экологически безопасным и экономичным.
Проводятся серологические исследования всем донорам перед забором тканей.
Серологические исследования на антитела к бледной спирохете:
- Экспресс - анализ;
- Реакция связывания комплемента.
Серологические исследования на маркеры вирусных инфекций:
- HBsAg;
- AntiHCV;
- Антитела к ВИЧ.
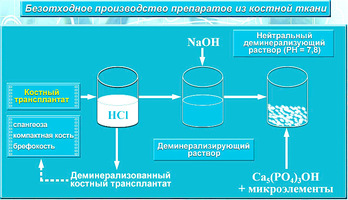
3. Оригинальный технологический комплекс многостадийной очистки материала Лиопласт
При изготовлении «Биоимплантаты костные аллогенные механически и ультразвуком обработанные лиофилизированные стоматологические стерильные «ЛИОПЛАСТ»® применяется оригинальный алгоритм изготовления из кадаверных тканей.
В процессе производства используются преимущественно физические факторы, а применение химических реагентов сведено к минимуму.
На первом этапе процесс получения биоимплантатов включает специальную ультразвуковую обработку тканей для удаления элементов костного мозга и жира, проведения первичной стерилизации материала, вирусной инактивации.




После первичной обработки ткани лиофилизируют, а затем герметично упакованный материал стерилизуют радиационным способом.
Обработка биоимплантатов с помощью физических факторов:
- Ультразвук 26 – 40 кГц
- Лиофилизация
- Гамма – стерилизация (стерилизация быстрыми электронами).
4. Тенические требования, требования к безопасности и качеству материалов, стерилизации
Биоимплантаты должны соответствовать требованиям технических условий и изготавливаться по технологическому регламенту № 028, утвержденному в установленном порядке.
Биоимплантаты должны быть изготовлены на основе ткани аллогенной природы.
Заготовка и обработка биоимплантатов производится согласно Приложению к приказу Министра здравоохранения СССР от 14 июня 1972г. № 482.
Биоимплантаты должны изготавливаться в соответствии с формой, размерами и объемом, согласно ТУ:
- Поверхность биоимплантатов должна быть без трещин, без отломов и раковин.
- Цвет костных биоимплантатов должен быть белый, серый или слоновой кости.
- Относительное содержание липидов в губчатой костной ткани – (1,2 ±1)%.
- Содержание влаги в биоимплантатах должно быть не более 5%.
- Водородный показатель (рН) биоимплантатов должен быть в пределах 4,0-8,0 рН.
- Дисперсность порошка должна находиться в пределах 103-101.
- Биоимплантаты должны быть стерильными.
Метод стерилизации – радиационный. Доза стерилизации (20,0±5,0) кГрей.
Индивидуальная упаковка биоимплантатов должна быть герметична.
Биоимплантаты при транспортировании должны быть устойчивы в транспортной упаковке к воздействию климатических факторов для условия хранения 5 (ОЖ4) ГОСТ 15150.
Биоимплантаты при транспортировании должны быть устойчивы в транспортной упаковке к воздействию механических факторов (вибрационные нагрузки: диапазон частот 10-55 Гц, амплитуда перемещения 0,35 мм; ударные нагрузки: пиковое ударное ускорение 10g, длительность действия ударного ускорения 16 мс).
Средний срок годности биоимплантатов должен быть 3 года.
5.Гарантии производителя. Безусловные и обусловленные гарантии. Ответственность

Предприятие-изготовитель гарантирует соответствие биоимплантатов «Лиопласт» всем требованиям настоящих технических условий при соблюдении условий транспортирования, хранения, эксплуатации, установленных настоящими техническими условиями.
Гарантийный срок годности 3 года с момента стерилизации.
Гарантийная программа Лиопласт на биоимплантаты и компоненты
1. Гарантии на биоимплантаты «Лиопласт» и компоненты.
1.1 Гарантия на биоимплантаты. Компания «ЛИОСЕЛЛ» предоставляет гарантию на период всего срока годности биоимплантатов с даты проведения стерилизации.
1.2. Гарантия на компоненты биоимплантатов «Лиопласт». Компания «ЛИОСЕЛЛ» предоставляет гарантию на период всего срока срока годности биоимплантатов с даты проведения стерилизации.
1.3. Изъятия из гарантии. Гарантии, предусмотренные настоящим документом, распространяются только на воспроизводимые и удостоверяемые дефекты и не распространяются на продукцию: биоимплантаты, их компоненты или иные продукты или любые услуги, предоставленные кем-либо кроме компании «ЛИОСЕЛЛ», а также представительств «ЛИОСЕЛЛ», указанных на официальном сайте lyoplast.com.
2. Предоставление гарантий и гарантийная поддержка.
2.1. Дата начала предоставления гарантий. Для пользователей биоимплантатов «Лиопласт» период предоставления Гарантий начинается с первого дня после поставки товара.
Для пользователей, приобретающих продукцию в интернет-магазине или посредством личного контакта выдается гарантийный сертификат для конкретного пациента при каждой покупке.
2.2. Уведомление. Пользователь биоимплантатов «Лиопласт» обязан должным образом уведомлять по телефону или электронной почте Компанию «ЛИОСЕЛЛ», а также представительства «ЛИОСЕЛЛ», указанные на официальном сайте lyoplast.com напрямую о любой проблеме, связанной с биоимплантатами и компонентами, а также предоставлять информацию, достаточную для установления истинных причин проблемы.
2.3. Поддержка по единому телефону (964) 342-16-12.
Служба клинической поддержки по телефону доступна бесплатно с 9:00 до 18:00 по местному времени для всех пользователей биоимплантатов «Лиопласт», которые работают на территории Российской Федерации, действующие на момент обращения.
После получении запроса служба поддержки диагностирует проблему и предложит решение по телефону.
Если этого будет недостаточно для принятия рационального решения, подпадающего под действие актуального Договора поставки и Служба клинической поддержки не может решить проблему дистанционно, то будет назначена дата встречи представителя компании «ЛИОСЕЛЛ» с врачом и пациентом для выяснения причин и заполнения Анкеты на обмен биоимплантатов и компонентов.
3. Обязанности пользователя биоимплантатов «Лиопласт»
3.1. Право пользователя биоимплантатов «Лиопласт» на Гарантии в соответствии с данным документом имеет место только в случае соблюдения пользователем биоимплантатов «Лиопласт» следующих обязательств:?
- обеспечивать выполнение операций в соответствии с рекомендованным протоколом имплантации и с применением необходимых инструментов и оборудования,
- содержать в надлежащем состоянии инструменты и и оборудование, обеспечивать качественную и тщательную очистку и химическую обработку, правильную стерилизацию в соответствии с официальными рекомендациями производителей;
- не производить никаких изменений и не применять с продуктами не имеющими отношения к биоимплантатам «Лиопласт» без предварительного письменного согласия Компании «ЛИОСЕЛЛ»,
- содержать биоимплантаты «Лиопласт», их компоненты в чистоте и целостности, использовать их должным образом и бережно в соответствии с инструкциями по применению, разработанными Компанией «ЛИОСЕЛЛ», а также не допускать к работе с биоимплантатами и компонентами не уполномоченных на это и не подготовленных сотрудников;
- содержать наружные поверхности упаковки биоимплантатов и компонентов в чистом виде и в нормальных условиях,
- не пытаться приспосабливать либо модифицировать биоимплантаты «Лиопласт» и не просить, разрешать или уполномочивать кого-либо кроме Компании «ЛИОСЕЛЛ» а также других представительств «ЛИОСЕЛЛ», указанных на официальном сайте lyoplast.com, осуществлять такое приспособление для работы с биоимплантатами «Лиопласт»,
- использовать биоимплантаты, их компоненты только для проведения операций имплантации, хирургических процедур и манипуляций с продуктами «Лиопласт»,
- не использовать никакие аксессуары, приложение или дополнительное оборудование, кроме тех, которые были предоставлены или письменно утверждены Компанией «ЛИОСЕЛЛ».
3.2. Изменения. Компания «ЛИОСЕЛЛ» может, по своему усмотрению, предоставлять пользователю определенные конструктивные и технологические "Изменения" биоимплантатов «Лиопласт» и их компонентов, а пользователь биоимплантатов «Лиопласт» настоящим обязуется должным образом использовать Изменения и в соответствии с предоставленными указаниями и инструкциями.
Компания «ЛИОСЕЛЛ» будет обновлять и пополнять продуктовую линейку биоимплантатов «Лиопласт» и регулярно сообщать пользователю в период действия актуального Договора поставки.
3.3. Регистрация на интернет-портале lyoplast.com .
Пользователь биоимплантатов «Лиопласт» обязан зарегистрироваться на сайте Компании «ЛИОСЕЛЛ» (lyoplast.com) указав данные регистрации в соответствии с электронной формой, что является обязательным условием предоставления Гарантии пользователю биоимплантатов «Лиопласт».
При отсутствии такой регистрации Компания «ЛИОСЕЛЛ» вправе отказаться от исполнения настоящего Гарантийной программы «Лиопласт» на биоимплантаты и их компоненты полностью или частично.
3.4. Конечный пользователь биоимплантатов и их компонентов.
Пользователь биоимплантатов «Лиопласт» гарантирует, что он является конечным пользователем биоимплантатов «Лиопласт» и их компонентов, приобретенных или полученных в пользование в соответствии с актуальным Договором поставки, и что продукция (биоимплантаты, их компоненты, и прочие продукты и услуги Компании «ЛИОСЕЛЛ» а также других представительств «ЛИОСЕЛЛ», указанных на официальном сайте lyoplast.com, приобретены не с целью перепродажи или дистрибуции, а также обязуется не выделять, переуступать или передавать каким-либо образом кому-либо биоимплантаты, их компоненты и прочие продукты и услуги Компании «ЛИОСЕЛЛ» а также других представительств «ЛИОСЕЛЛ», указанных на официальном сайте lyoplast.com, или Гарантии без письменного согласия Компании «ЛИОСЕЛЛ» а также других представительств «ЛИОСЕЛЛ», указанных на официальном сайте lyoplast.com.
Права пользователя биоимплантатов «Лиопласт» по актуальному Договору поставки не могут быть переданы третьим лицам без согласия Компании «ЛИОСЕЛЛ» а также других представительств «ЛИОСЕЛЛ», указанных на официальном сайте lyoplast.com.
4. Отказ от гарантий.
Прекращение действия обязательств Компании «ЛИОСЕЛЛ» а также других представительств «ЛИОСЕЛЛ», указанных на официальном сайте lyoplast.com
4.1. Компания «ЛИОСЕЛЛ» не несет гарантийные обязательства и не производит бесплатный обмен биоимплантатов и их компонентов в следующих случаях:
- если изделие, предназначенное для личных нужд, использовалось в иных целях, не соответствующих его прямому назначению;?
- нарушения правил и условий эксплуатации установки изделия, изложенных в Сертификате качества «Лиопласт» и другой документации, передаваемой пациенту в комплекте с изделием;
- если изделие имеет следы попыток неквалифицированной коррекции;?
- если осложнение вызвано проведенным лечением, выполненным в другой клинике;
- если осложнение вызвано вызван действием непреодолимых сил, несчастными случаями, умышленными или неосторожными действиями потребителя или третьих лиц;?
- если обнаружены механические повреждения, возникшие после передачи изделия конечному пользователю; повреждения, вызванные воздействием влаги, высоких или низких температур, коррозией, окислением, попаданием внутрь изделия посторонних предметов, веществ, жидкостей, других предметов;
- если дефект возник вследствие естественного износа при использовании изделия и утрачена его упаковка.
При этом под естественным износом понимаются последствия использования изделия, вызвавшие ухудшение их функционального состояния и внешнего вида из-за длительного активного использования данного изделия; Компания «ЛИОСЕЛЛ» не несет ответственность за возможный вред, прямо или косвенно нанесенный изделием людям, домашним животным, имуществу в случае, если это произошло в результате несоблюдения правил и условий эксплуатации, установки изделия; умышленных или неосторожных действий покупателя (конечного пользователя) или третьих лиц.
Для получения гарантийного обмена биоимплантатов и их компонентов вы можете обратиться по телефону поддержки +7(964) 342-16-12 или другим, указанным в Гарантийном талоне.
Научная основа и перспективные разработки связанные с пластическими материалами Лиопласт
За время существования Самарского Банка Тканей все виды костно-замещающих материалов по технологии «Лиопласт» прошли клиническую апробацию во многих городах России и ЕЭС.
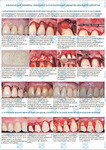
Врачи применяют материалы в стоматологии: при удалении зубов для консервации лунок, в пародонтальной хирургии, при имплантации зубов, костной пластике, для лечения периимплантитов, пародонтитов; для увеличения объема кости челюсти по ширине и высоте, в ортодонтии.
В челюстно-лицевой хирургии и травматологии биоимплантаты «Лиопласт» используются для протезирования целых костей, замещения нижней челюсти, при обширных травмах и резекциях.
Ежегодно появляются новые патенты по видам материалов Лиопласт и способам их применения.
В настоящее время ведутся разработки новых форм выпуска продукции (кольцевидные блоки, костные конусы, изогнутая твердая мозговая оболочка и многие другие) для максимальной индивидуализации биоимплантатов и упрощения операции костной пластики и имплантации зубов.
Для стандартных изделий планируется изменение упаковки на более удобную (разовые шприцы).
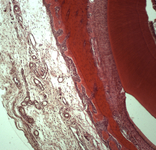
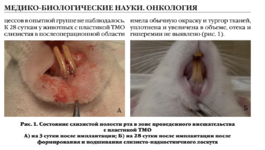
Плотное взаимодействие с сотрудниками вивария, биотехнологической и гисто-морфологической лабораториями помогают в научном изыскании, а также подтверждении лабораторных и первичных клинических результатов в экспериментах на животных и при гистологических исследованиях.
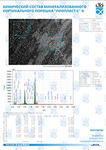
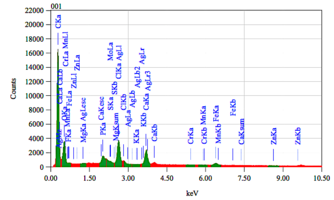
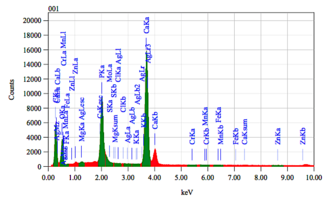
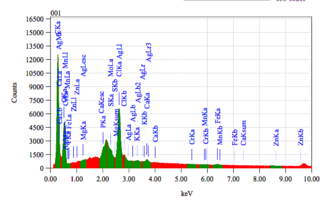
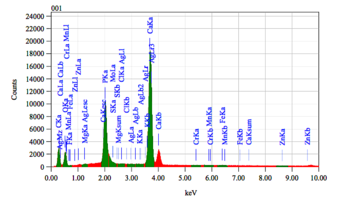
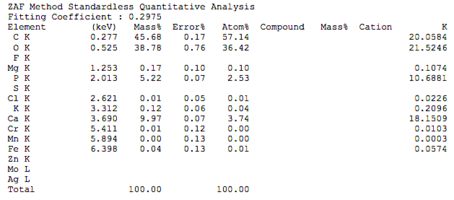
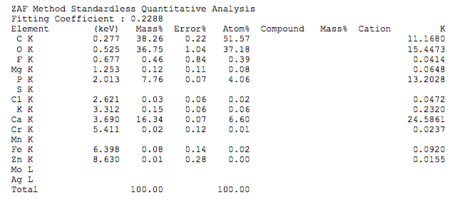
Химический состав деминерализованного кортикального порошка.pdf
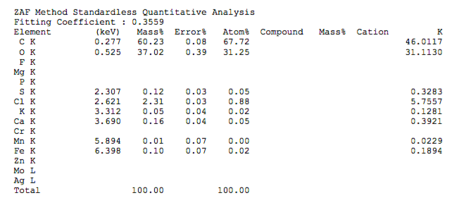
Химический состав деминерализованной спонгиозного порошка.pdf
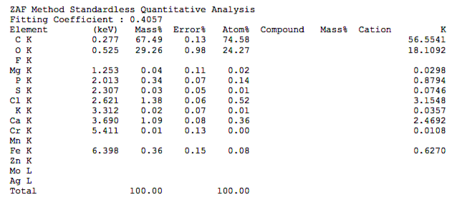
Химический состав минерализованного спогиозного порошка.pdf
Химический состав минерализованного кортикального порошка.pdf
Приоритетная справка хирургическая методика для индивидуальных костных блоков.pdf
Приоритетная справка фармакотерапевтическое сопровождение костной пластики.pdf