+7 (929) 727 53 60 Травматология / Ортопедия
Банк аллогенных тканей и научно-исследовательский институт "БИОТЕХ" СамГМУ
- Cамарский банк тканей основан на базе Центральной научно-исследовательской лаборатории (ЦНИЛ), в настоящее время Научно-исследовательский инстутут "БиоТех" Самарского государственного медицинского университета (СамГМУ).
- В 2023 году Самарский Банк Тканей отметил своё 40-летие, а ЦНИЛ - 60-летие.
- «ЛИОСЕЛЛ» - это малое инновационное предприятие, созданное на базе Самарского медицинского университета.
- «ЛИОПЛАСТ» - продукция компании «ЛИОСЕЛЛ».
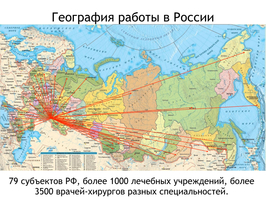
- Биоимплантаты, используются в 80 регионах России, 135 городах и более чем в 1000 лечебных учреждений.
Производство биоимплантатов "Лиопласт®" организовано в Самарском Государственном Университете при участии Центральной научно-исследовательской лаборатории и Самарского банка тканей, являющихся структурными подразделениями Университета.
В Самарском банке тканей применяется оригинальный алгоритм изготовления биопрепаратов из тканей человека, защищенный патентами РФ.
Биоимплантаты, получаемые по технологии "Лиопласт®" состоят только из компонентов человеческого организма, не содержат внесенных извне химических веществ.
В процессе производства используются преимущественно физические факторы, а применение химических реагентов сведено к минимуму.
Всем донорам проводится аутопсия и серологическое исследование крови на сифилис, вирусы гепатитов В и С, СПИД.
Технологии производства биоимплантатов "Лиопласт®" позволяют полностью защитить реципиента от передачи ему какого-либо заболевания, сводят до минимума опасность инфицирования персонала и делают процесс экологически безопасным и экономичным.
Костнопластический материал применяется в виде порошков, крошки, цилиндров, блоков, клиньев, полосок, крупных фрагментов.
Выпускаются деминерализованные костные порошки и блоки из аллокости. Биоимплантаты также изготавливают из сухожилий, твердой мозговой оболочки, фасций.
Процесс заготовки тканей изначально и по настоящее время разделен на два этапа, в отличие от работы других банков тканей нашей страны.
Забор кадаверного материала проводится сотрудником банка на базе бюро судебно-медицинской экспертизы, а последующая обработка – в отделении консервации банка тканей, в который материал поступает только после получения результатов серологических исследований крови донора.
На первом этапе процесс получения имплантатов включает специальную ультразвуковую обработку тканей для удаления элементов костного мозга и жира из спонгиозы, проведения первичной стерилизации материала и вирусной инактивации.
После первичной обработки ткани лиофилизируют, а затем герметично упакованный материал стерилизуют радиационным способом.
Кроме того, использование низкочастотного ультразвука при очистке материала позволяет не повреждать нативную структуру соединительных таней, сохраняя все биологические потенции и активности биоимплантатов Лиопласт.
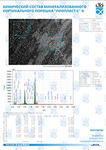
В рамках замкнутого цикла безотходного производства специалисты в банке тканей одновременно получают два вида новых материалов: деминерализованные костные формы и минеральный компонент костной ткани человека - "аллогенный гидроксиаппатит".
Полученный минералосодержащий комплекс кроме солей кальция и фосфора содержит и другие микроэлементы (железо, магний, кобальт, цинк, серебро), а также глюкозаминогликаны в тех же пропорциях, в каких они находятся в костной ткани человека (коллаген и хондроитина сульфат).
Разработанный университетом принцип дифференцированного подбора костных биоимплантатов, основу которого составляют анатомо-гистологические и регенераторные потенции поврежденных эпителиальных и соединительных тканей, обеспечивает полную регенерацию поврежденной костной ткани пациента и сохранение анатомической целостности органа.
Использование новых и уже известных видов имплантатов в сочетании с предложенными методиками регулирования послеоперационных процессов, позволило на 10-12% сократить время лечения больных по сравнению с традиционными методами, повысить процент успешного выздоровления (например, при переломе шейки бедренной кости у пожилых людей) на 44%.
Вместе с клиницистами различных специализаций (стоматологами, оториноларингологами, офтальмологами, травматологами, ортопедами, онкологами, гнойными и пластическими хирургами, комбустиологами) разработаны новые способы малоинвазивных и малотравматичных органосохранных операций с применением аллогенных биопрепаратов и физиотерапевтических средств в комплексном лечении больных с патологией опорно-двигательной системы, зубочелюстной области, кожных покровов, зрения и слуха, для лечения остеопороза.
Оригинальные операции с использованием видеоэндоскопической техники и биоимплантатов применяются в спортивной медицине.
Использование лиофилизированных аллотканей «Лиопласт"® показало их высокую эффективность при комплексном хирургическом лечении многих заболеваний у лиц различных возрастных групп.
На сегодняшний день результаты аллогенных пересадок с использованием наших материалов и методик вплотную приближаются к результатам при аутопластике. При этом не наблюдается нарушений гомеостаза, стрессовых и посттравматических осложнений, связанных с забором собственных тканей организма.
2. Историческая динамика ЦНИЛ СамГМУ с момента организации отделения консервации тканей
Насущная необходимость в открытии тканевого банка в Куйбышеве (ныне город Самара) появилась еще в 70-годы прошлого века.
В тот период в Куйбышевском Медицинском Институте активно развивались травматология и стоматология, поэтому потребность в биологическом материале была очевидной.
Идея организовать Банк тканей в медицинском ВУЗе принадлежит академику РАМН Александру Федоровичу Краснову, руководившему в то время институтом и кафедрой травматологии и ортопедии. Предпринимались неоднократные попытки открыть такую структуру.
Но только после того, как профессор Владимир Николаевич Шляпников, проректор института, заведовавший Центральной научно-исследовательской лабораторией с 1970 по 1977 годы, патологоанатом по специальности, предложил развернуть банк тканей на базе Центральной научно-исследовательской лаборатории Куйбышевского медицинского института, дело сдвинулось с мертвой точки.
Банк тканей был организован в 1983 году. В начале существования он представлял собой одно подразделение – Отделение консервации тканей. Его открытие датировано приказом по КМИ и областному отделению здравоохранения № 285/48 от 18 августа 1983 года.
С 2000 года в структуре банка тканей организована лаборатория культивирования клеток, внутри которой функционируют две отдельные лаборатории: клеток животных и клеток человека.
6 марта 2002 года Отделение консервации тканей было переименовано в Самарский банк тканей (приказ №40 по СамГМУ). Куйбышевский банк тканей стал единственным в стране, находящимся в структуре высшего учебного заведения.
В первое десятилетие работы Куйбышевского банка тканей для изготовления биопрепаратов использовали жидкие консервирующие среды, в частности отечественный метод консервации в слабых растворах формалина (Парфентьева В.Ф. с соавторами).
Этот доступный, недорогой и эффективный способ позволяет одновременно консервировать и стерилизовать материал.
Кроме того, как показали наши собственные исследования, консервированные таким образом биологические ткани приобретают дополнительный антимикробный эффект.
Однако срок годности их ограничен до полугода, имеются сложности с транспортировкой, требуется постоянный температурный режим хранения (+40С).
Поэтому возникла необходимость производить костно-пластический материал с большими сроками хранения и возможностью их простого применения в клинической практике.
В дальнейшем Самарский банк тканей перешел на способ консервации путем лиофилизации тканей с применением сублимационной установки с последующей радиационной стерилизацией гамма-лучами, а в последнее время – быстрыми электронами.
Этот метод позволяет сохранять биологический эффект тканей до 5 лет и более, складировать их в обычных помещениях и переправлять в любую точку страны и мира без применения специальных условий доставки.
Наши научно-практические наработки позволили выйти на международный уровень. В 1992 году был подписан первый международный контракт с Испанией.
Благодаря зарубежным инвестициям стало возможно расширить исследования в области тканевой инженерии и реализовывать инновационные проекты.
С 1992 года было организовано высокотехнологичное производство лиофилизированных биоимплантатов.
В результате наши новые технологии изготовления биоматериалов были запатентованы, зарегистрирована торговая марка (свидетельство № 265748), биоматериалы «Лиопласт» были занесены в федеральный реестр изделий медицинского назначения (РУ №ФСР 2010/08120; Сертификат № РОСС RU ИМ 02.В16812) и разрешены к применению в клинической практике на территории РФ.
Именно научно-техническая база в то время ЦНИЛ, а ныне НИИ "БиоТех", включающая в себя блок научно-исследовательских лабораторий фундаментального плана, экспериментальный отдел, виварий, отличные условия для проведения экспериментов на животных и культурах клеток, обеспечила реализацию инновационных проектов Самарского банка тканей и всесторонние доклинические испытания новых биогенных образцов.
В настоящее время для лечебных целей в Самарском банке тканей изготавливают около 100 видов имплантатов «Лиопласт» - практически из всех видов соединительных тканей, разнообразных по форме, объему биоматериала в упаковке.
Их получают из зрелой пластинчатой костной ткани губчатой и компактной формаций, незрелой брефокости, хрящей, сухожилий, фасций, твердой мозговой оболочки, а также раньше плаценты и амниона.
Основную массу продукции «Лиопласт» составляют костно-пластические материалы. Препараты выпускаются в виде блоков, цилиндров, пластин, полосок, крошки, порошков.
Научно-исследовательский институт "БИОТЕХ" занимается проблемами регенеративной медицины уже 60 лет и более 40 лет существует Банк тканей СамГМУ.
Банк тканей следует признать российским достижением, т.к. в отличие от других банков он был создан на базе ВУЗа с целью создания запасов алломатериалов для клиники, разработки новых технологий, что изначально подразумевало его инновационный принцип.
В настоящее время его деятельность вышла далеко за пределы СамГМУ в другие регионы РФ, а также ближнего и дальнего зарубежья.
Изначально в основу работы Самарского Банка тканей положен принцип разделения производственных зон с забором нестерильного донорского материала.
Это стало возможным благодаря разработанному и внедренному нами в практику оригинального запатентованного метода технологического процесса, включающего в себя проведение специальной обработки кадаверных тканей, первичное обеззараживание, в том числе вирусную инактивацию биологического материала, его консервации методом лиофилизации.
При этом особое значение придается применению в основном физических факторов воздействия на биоматериал и сведение химических веществ к минимуму.
Огромное значение в снижении трудоемкости заготовки с соблюдением принципов экологичности приобрело введение в технологический процесс ультразвукового низкочастотного модуля, который позволяет не только обезжирить и очистить от крови и других видов соединительной ткани спогиозу, провести первичную стерилизацию биоматериала, но и создать линейку продуктов с пролонгированными антибактериальными и антифунгицидными свойствами.
Стерилизация готовой продукции за рубежом осуществляется окисью этилена.
В Самарском банке тканей эта проблема решена за счет радиационных методов, опыт их применения насчитывает уже 20 лет.
Только в последние годы мировая практика заготовки аллотканей человека показала преимущество радиационных методов, что стало «золотым стандартом».
Благодаря расположению Банка тканей на базе НИИ "БИОТЕХ" с имеющимися подразделениями и являющегося структурным подразделением СамГМУ стало возможным проведение фундаментальных исследований регуляции регенераторных процессов в опорных и покровных тканях человека и животных с дифференцированным применением продуктов клеточных и тканевых биотехнологий.
Все исследования проводятся по двухэтапному принципу – in vitro и in vivo с применением оригинальных экспериментальных моделей и комплексным подходом в оценке полученных результатов с применением современных методов анализа.
Характерной особенностью нашего времени является развитие реконструктивной и регенеративной медицины.
В травматологии, ортопедии, стоматологии, онкологии и гнойной хирургии изыскание подходов к лечению патологии опорных и покровных тканей организма человека и предполагает не только средства её устранения, но и достижения первоначальной формы, структуры и функции разрушенных травмами и болезнями костей.
Обеспечение полной регенерации костной ткани в области дефектных участков кости, несмотря на накопленные знания в этом вопросе - одна из острейших проблем современной медицины.
Решить ее можно, создав оптимальные условия для регенераторных процессов в зонах ее резорбции. Один из путей - использование костнопластических материалов.
Тканевые биоинженерные технологии и тканевая терапия, применение различных компонентов тканей человека являются общепризнанными высокоэффективными методами реконструктивной и регенеративной хирургии.
Современный уровень развития науки и техники позволяет при повреждениях и разрушениях опорных и покровных тканей организма производить их полное восстановление с помощью препаратов биогенной природы.
Среди них аллогенные имплантаты из кадаверных тканей человека являются оптимальными материалами для реконструкции повреждений опорно-двигательной системы.
При их применении, в отличие от ауто- и ксенопластики и использования синтетических препаратов, не нарушается гомеостаз и метаболизм соединительных тканей и функции систем жизнеобеспечения реципиента.
Расширение объема хирургического пособия, связанное с получением у больного человека костного аутотрасплантата, не только усугубляет течение послеоперационного периода, но и вызывает значительные нарушения в организме.
Аутопластика невозможна лицам с системными заболеваниями костной ткани, детям и пожилым людям. Результаты же оперативных вмешательств с применением аллогенных биоимплантатов при определенных условиях не уступают остеопластике с использованием собственных тканей больного.
При рациональном способе применения такие биоимплантаты обеспечивают репаративный характер регенерации, реализуя генетические возможности самого организма – способности соединительных тканей к их полной регенерации.
Проблемами заготовки тканей человека и разработкой способов рационального использования в клинике занимаются как в нашей стране, так и за рубежом специальные медицинские учреждения – тканевые банки.
Деятельность банков тканей направлена на образование запасов биологических материалов и обеспечение ими специализированных лечебных учреждений.
Другой, не менее важной задачей является научно-исследовательская работа, цель которой – решение насущных проблем фундаментальной и прикладной биоимплантологии.
Таким образом, сами задачи банков тканей определяют инновационный характер их деятельности.
Это подтверждают и результаты научно-практической деятельности Самарского банка тканей, который активно проводит новые разработки в области тканевых и клеточных технологий с коммерциализацией научных идей.
4. Интервью с Ларисой Теодоровной Воловой, директором ЦНИЛ СамГМУ. 6 Февраля 2014 года. День науки
Алексей Шаров: Добрый день, дорогие друзья! Сегодня мы в городе Самаре и будем говорить об отечественном инновационном продукте. Это биоимплантаты «Лиопласт-С»® (Lyoplast)®. И поможет нам в этом автор и разработчик, - Лариса Теодоровна Волова, доктор медицинских наук, профессор, академик РАЕ, директор ИЭМБ (Института Экспериментальной медицины и Биотехнологий) Самарского Государственного Медицинского Университета.
Алексей Шаров: Лариса Теодоровна, существуют ли в Вашем институте приоритетные направления?
Лариса Теодоровна Волова: В стенах ИЭМБ занимаются различными направлениями в области биотехнологий. Свыше 30 лет мы работаем в области тканевых технологий, около 12 лет в области клеточных технологий и 7 лет в области нанотехнологий.
В частности, разработаны такие новые медицинские технологии для регуляции процессов остеогенеза при замедленной консолидации и пародонтите, остеопорозе, ожогах кожи, травмах. Наши продукты используются для создания клеточно-тканевых трансплантатов для хондропластики и исследований в космической медицине.
Они являются не только переносчиком клеток, но и биореактором, а также способны выполнять формообразующие и генетические функции.
Также нами разработаны технологии получения и стандартизации культур клеток из стромы различных органов и тканей животных и человека; методология тестирования различных лекарственных препаратов и средств медицинского назначения, физиотерапевтических факторов in vitro.
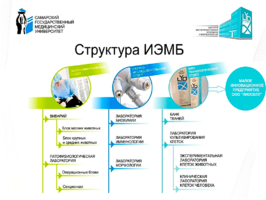
Наши приоритетные направления в институте: регенеративная медицина и критические биотехнологии. У нас имеются три лаборатории для фундаментальных исследования: биохимии, иммунологии и морфологии. Биотехнологический отдел имеет банк тканей, две лаборатории: культивирования клеток животных и человека.
Алексей Шаров: Какими качествами обладает материал "Лиопласт-С"®?
Лариса Теодоровна Волова: Аллогенные имплантанты из кадаверных тканей человека идеально подходят для реконструкции повреждённых тканей опорно-двигательной системы, т.к. они не оказывают негативного влияния на гомеостаз и метаболизм соединительных тканей и функции систем жизнеобеспечения реципиента.
Чего нельзя сказать о синтетических препаратах, ауто- и ксенопластических материалах.
Аллогенные материалы, взятые у донора того же биологического вида после их специальной обработки практически полностью теряют свою антигенность и не оказывают негативного воздействия на организм, в который они помещены.
Они становятся матрицей (кондуктором), а деминерализованные имплантаты еще и индуктором остеогенеза. Биоимплантаты постепенно полностью рассасываются, а на их месте формируется новая органотипичная костная ткань реципиента.
Во всех случаях биоимплантант содержит остеоиндуктивные протеины(морфогенетические белки), которые стимулируют, например, митогенез (деление) недифференцированных периваскулярных (адвентициальных) клеток в остеопрогениторные мезенхимальные клетки, которые затем превращаются в остеобласты и дают начало новой костной ткани.
Наш материал известен за рубежом более двадцати лет. С 1992-го по 2000 имеется опыт работы с партнерами из Испании. Однако длительная процедура вступления России в единый торговый союз и ВТО тормозила проникновение материала на мировой рынок.
Кроме этого, существовал министерский запрет на экспорт человеческой ткани и биологических объектов, под который мы также попали. Сегодня эти барьеры сняты и мы имеем несколько десятков предварительных контрактов с отечественными и западными компаниями.
А творческими и деловыми связями мы объединены с 80-тью регионами нашей большой и прекрасной страны.
Алексей Шаров: Почему Вы предпочитаете изготавливать биоимплантанты из тканей человека?
Лариса Теодоровна Волова: Кадаверный человеческий материал предпочтителен по целому ряду факторов.
Во-первых, это гомологичный материал.
Он полностью идентичен по своей структуре и биохимическому составу, а также процессам и механихмам рассасыания и замещения новой тканью.Всематериалыимеютчетковыраженнуювидовуюспецифичность.
Так, например, морфогенетические белки свиньи, лошади или коровы никогда не вызовут миграцию клеток в очаг воспаления и эктопического остеогенеза в организме человека.
Не говоря о синтетических материалах. По этой причине применение последних серьезно ограничено в клиническом аспекте по биологическим и физиологическим причинам.
Во-вторых, проводимые исследования в этом направлении с человеческими тканями более 50 лет во всём мире позволили выявить вероятные и наиболее характерные болезни и способы их нейтрализации при производстве биоимплантатов.
Чего нельзя сказать о тканях животных: коров, свиней, обезьян, лошадей.
Губчатый энцефалит и прочие заболевания встречаются у многих животных, а корова - вообще в этом плане опасное животное: более чем у 80 % поголовья встречаются лейкозы.
Методов анализа большинства заболеваний животных не существует, следовательно, не представляется возможным прогнозировать поведение животных тканей в человеческом организме и последствий от этого для здоровья пациента.
В - третьих, на доноров законодательно (с 1992 года) распространяется презумпция согласия.
То есть, не требуется разрешения родственников на использование тканей скоропостижно скончавшегося человека в возрасте 18-60 лет, кроме случаев, когда имеется письменное заранее представленное несогласие или этот отказ регламентирован завещанием потенциального донора.
Наконец, в-четвёртых, безопасность использования трупного человеческого материала обеспечивается 6-ю степенями защиты и многостадийной предварительной очисткой и обработкой.
Алексей Шаров: Как осуществляется отбор и обработка человеческого материала?
Лариса Теодоровна Волова: Отбор, самый тщательный и скурпулёзный, начинается с выбора доноров.
Больные и агонизирующие пациенты не рассматриваются. Остальные доноры проверяются на вирусы (СПИД, гепатит В, С), сифилис. Всем проводится аутопсия. Донорами являются только внезапно скончавщиеся от травмы, механической асфиксии и сердечно-сосудистой патологии люди.
Заготовленный материал подвергается специальной обработке в основном физическими способами (механическим, ультразвуковым, вакуумным, радиационным и т.п.). В качестве химических средств используются только растворители для финального обезжиривания и деминерализации, и то их применение в крайней степени ограничено.
Технология практически на 100% исключает попадание следовых количеств чужеродных и технологических веществ и растворителей. Готовый материал упаковывается, стерилизуется радиацией и хранится при комнатной температуре в сухом прохладном месте.
Алексей Шаров: В Европе и в США банки тканей предоставляют не только стандартные продукты, но и индивидуальные имплантаты. Как обстоят дела у Вас?
Лариса Теодоровна Волова: Помимо ста видов стандартных продуктов, например, в виде блоков, цилиндров, спонгиозного порошка или крошки (минерализованной или деминерализованной) из костной ткани, мы производим персонифицированные продукты.
Вот уже как 2 года мы имеем возможность изготавливать высокоточные индивидуальные костные блоки для стоматологии, используя данные компьютерной томографии челюстей пациента для моделирования индивидуальной блока и последующего его выпиливания на специализированном станке.
Алексей Шаров: Сколько людей заняты на Вашем производстве?
Лариса Теодоровна Волова: Не более 15 человек. Наши технологии и оборудование позволяют производить материал в промышленных объёмах, не привлекая при этом дополнительного персонала.
Все сотрудники имеют высокую квалификацию и прошли необходимое обучение и стажировки.
Алексей Шаров: Какие технические новшества можно будет ожидать в недалёком будущем?
Лариса Теодоровна Волова: Развитие направления индивидуальных имплантатов для офтальмологии, травматологии, ЛОР-хирургии.
Создание комбинированных клеточно- тканевых трансплантатов.
Алексей Шаров: Где и как можно ознакомиться более детально с Вашим продуктом?
Лариса Теодоровна Волова: Прежде всего на наших сайтах http://lyoplast.com, http://lyoplast.ru и http://russianboneblocks.ru и у наших ключевых дилеров.
Нашими клиническими представителями в России являются Алексей Шаров и Мария Носова из Санкт-Петербурга.
Они оба являются авторами патентов по нашим материалам, занимаются научными исследованиями и могут предоставить подробные и исчерпывающие консультации по использованию материалов в различных клинических случаях.
Алексей Шаров: Лариса Теодоровна, спасибо Вам за обстоятельные пояснения, поздравляем Вас и Ваш коллектив с Днем Науки, желаем Вашему коллективу дальнейших творческих успехов и до следующей встречи!