+7 (929) 727 53 60 Травматология / Ортопедия
Банк аллогенных тканей и научно-исследовательский институт "БИОТЕХ" СамГМУ
НИИ «БиоТех» - структурное подразделение Самарского государственного медицинского университета (СамГМУ), инфраструктурный мультидисциплинарный кластер, реализующий научно-исследовательские, образовательные и инновационные медицинские направления, а также производство в сфере биотехнологий и персонифицированной медицины на международном уровне.
Одним из направлений работы НИИ «БиоТех» СамГМУ является проведение доклинических исследований по авторской двухступенчатой методике на клетках in vitro и лабораторных животных in vivo. Точные данные и широкие возможности!
Подразделения и направления исследований НИИ «БиоТех»
Отдел клеточных технологий (клеточные биотехнологии):
- Лаборатория получения первичных культур клеток из разных источников тканей человека и животных с криобанком;
- Лаборатория создания биомедицинских клеточных продуктов и клеточных линий;
- Лаборатория 3D-биопринтинга;
- Лаборатория создания универсальных тест-систем;
- Лаборатория тестирования лекарственных препаратов, биоматериалов, физиотерапевтических факторов in vitro (ГОСТ Р, ISO, GLP).
Виварий и отдел доклинических испытаний:
- Виварий мелких, средних и крупных животных;
- Лаборатория тестирования лекарственных препаратов, биоматериалов и физиотерапевтических факторов in vivo на мелких, средних и крупных животных (ГОСТ Р, ISO, GLP);
- Лаборатория фундаментальных доклинических исследований (морфологических, биохимических, гематологических).
Участие в федеральных и международных проектах
Научные проекты:
- Программа стратегического академического лидерства «Приоритет-2030»;
- Национальная технологическая инициатива (НТИ) по сквозной технологии «Бионическая инженерия в медицине»;
- Исполнение государственного задания на выполнение научных работ.
Издательские проекты:
- Специальный выпуск "Biopolymers for Regenerative Medicine Applications" профильного индексируемого журнала Polymers, MDPI.
Отдел клеточных технологий НИИ «БиоТех» СамГМУ
- Разработаны технологии получения первичных культур (стволовых, прогениторных, дифференцированных) клеток человека и животных из разных источников – всего 8 популяций из 32 источников.
- Создан криобанк клеток, являющийся аналогом АТСС и функционирующий как в формате Master cell bank с клетками индивидуальных доноров и заморозкой на ранних пассажах (3-6), так и в формате Working cell bank с наращиванием объёма клеточной культуры (15-30 пассажей).
- Наши клеточные линии охарактеризованные, с прослеживаемой историей, их можно культивировать in vitro до 30 пассажей, что делает их практически сопоставимыми с бессмертными клетками.
- Преимущества наших клеточных продуктов заключаются в более низкой цене по сравнению с аналогами от ATCC. При этом объём продаваемого материала в случае ATCC составляет 0.5 млн. клеток, у НИИ «БиоТех» СамГМУ - 1-2 млн. клеток.
- Нами разработаны тест-системы на первичных культурах ювенильных клеток для сравнительной оценки in vitro эффективности новых биомолекул, биоаналогов и дженериков. Разрабатываются тест-системы на клетках крови человека для изучения патогенеза и персонифицированной медицины у пациентов с социально значимыми заболеваниями воспалительного генеза (ревматоидный артрит, подагра, псориаз) и органической патологией ЦНС (например, шизофрения).
- Впервые в мире внедрён информационно-термодинамический (фрактально-энтропийный) подход к оценке устойчивости воздействия внешних факторов на организованные клеточные системы при анализе эффективности и безопасности лекарственных средств и иных методов лечения (лучевой и другие физические факторы).
- В отделе создана новая клеточная биологическая модель для проведения исследований в космической медицине.
- Разработаны технологические процессы по созданию уникальных пионерских продуктов для 3D-биопечати (гидрогели и биочернила) и созданы технологии получения гибридных клеточно-тканевых продуктов.
Отдел доклинических исследований НИИ «БиоТех» СамГМУ
- Разработаны и внедрены в практику научно-исследовательской деятельности системы (ГОСТ Р, ISO, GLP) по двухступенчатому тестированию лекарственных препаратов и биоматериалов на безопасность и эффективность на первичных клеточных культурах (с определением гибели клеток морфологическими и биохимическими методами, оценкой пролиферативной активности и определением влияния исследуемого фактора на адгезивную способность клеток), а также на лабораторных животных (с использованием морфологических, биохимических, гематологических, лучевых (рентген, КТ, микроКТ) и визуализируемых (эндоскопия, ангиография) методов.
- Выполняется оценка противоопухолевого эффекта химических, биологических агентов и физиотерапевтических факторов на иммортализованных клетках, в том числе с анализом устойчивости выявленного эффекта с использованием информационно-термодинамического (фрактально-энтропийного) подхода;
- Выполняется анализ остеоинтеграции имплантатов на лабораторных животных с оценкой поверхности изделия, в том числе с использованием авторского пакета специализированных программ.
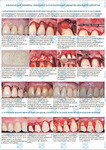
Дизайн исследования медицинских изделий (дентальных имплантатов) на безопасность, эффективность и биоинтеграцию. Исследования проходят по авторской двухступенчатой методике в соответствии с ГОСТ Р, ISO и GLP.
Наши партнёры и заказчики доказательных исслдований



.jpeg)














ООО «ПРОТОТИП» ООО «Найнтех»
Виды исследований и объём научной работы
|
Этап |
Биологический объект |
Исследуемые параметры |
Методы оценки |
|
I. Исследования in vitro на клетках
|
Мезенхимальные стромальные клетки костного мозга, дентальные фибробласты, эпителиальные клетки*
|
Жизнеспособность клеток на поверхности имплантата (цитотоксичность материала изделия) |
-Морфологический; -Иммуноморфологический с проведением люминесцентной микроскопии с флюорофорами; -Биохимический с проведением МТТ и ЛДГ тестов |
|
Пролиферативная потенция клеток на поверхности имплантата |
|||
|
Адгезивные свойства клеток и адгезия к поверхности имплантата |
|||
|
Оценка чистоты поверхности имплантата |
Сканирующая электронная микроскопия и (опционально) химический анализ поверхности изделия |
||
|
Статистический анализ полученных результатов с использованием авторского информационно-термодинамического (фрактально-энтропийного) подхода к оценке устойчивости воздействия внешних факторов на организованные клеточные системы |
|||
|
II. Исследования in vivo на лабораторных животных |
Крысы, кролики** |
Острая и (опционально) хроническая токсичность материала изделия |
-Морфологический; -Биохимический |
|
Биосовместимость |
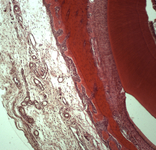
-Морфологический (гистологический) |
||
|
Биоинтеграция |
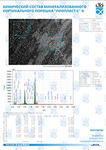
-Морфологический: анализ минерализованных гистологических препаратов – шлифов, содержащих фрагмент изделия и костной ткани, с оценкой характера биоинтеграции и подтверждением чистоты поверхности изделия |
||
*Используются собственные идентифицированные линии клеток человека, полученные в Лаборатории культур клеток НИИ БиоТех СамГМУ из первичного материала (биоптатов тканей здоровых людей). **Используются кролики породы советская шиншилла, крысы линии сток Wistar.
"Мы надеемся на интерес к нашему предложению и плодотворное взаимное сотрудничество! С уважением, профессор Волова Лариса Теодоровна", - Директор НИИ «БиоТех» СамГМУ
Химико-фармацевтические разработки в СамГМУ
- Отработка лабораторной технологии получения растительных экстрактов, индивидуальных БАВ природного происхождения;
- Подбор научно обоснованных композиций БАД, подготовка проектов ТУ, документов для регистрации;
- Отработка лабораторной технологии синтеза и производство высокомаржинальных мало- и средне тоннажных АФС;
- Получение интермедиатов для синтеза АФС, высокочистых образцов АФС и примесей к ним для контроля качества препаратов;
- Производство хроматографических колонок;
- Разработка и валидация методик, контроль качества субстанций синтетического и природного происхождения;
- Разработка и валидация методик определения концентраций ЛС в биологическом материале человека и животных;
- Моделирование различных значимых параметров (хроматографических, технологических и др.);
- Маркетинговый анализ ассортимента и объёмов продаж выбранной группы ЛС, обоснование выбора прототипа;
- Виртуальный скрининг, моделирование патентоспособных аналогов выбранных прототипов;
- Синтез субстанций молекул-кандидатов в ЛС с учетом ограниченного ассортимента и выбора исходных реагентов и материалов.
Доклинические исследования в СамГМУ
- Для оригинальных и воспроизведенных ЛС, физиотерапевтических факторов, ИМН и биомедицинских клеточных продуктов;
- Двухступенчатая авторская система тестирования на безопасность и эффективность на клеточных культурах in vitro и на животных in vivo в соответствии со стандартами ГОСТ, ISO, GLP;
- Изучение фармакокинетики и фамакодинамики ЛС, определение мутагенных, канцерогенных, эмбриотоксических и иных свойств исследуемых ЛС;
- Оценка острой и хронической токсичности ЛС, безопасности ИМН и биомедицинских клеточных продуктов;
- Собственный банк первичных клеточных линий с возможностью культивирования in vitro до 30 пассажей;
- Авторские клеточные тест-системы, предназначенные для сравнения биологической активности ЛС, их биосимиляров и дженериков;
- Оценка устойчивости воздействия внешних факторов на организованные клеточные системы авторским информационно-термодинамическим (фрактально-энтропийным) методом;
- Исследования на качество, безопасность и эффективность ЛС (в т.ч. биоэквивалентность ЛС), ИМН и биомедицинских продуктов, контактирующих с клетками и тканями реципиента на животных в экспериментально созданных патологических моделях in vivo;
- Индивидуальные параметры оценки испытываемых образцов в зависимости от экспериментальной модели и патологии.
Клинические испытания в СамГМУ
- Ведущий центр по проведению клинических исследований в России с более чем 20 летним опытом и портфолио из сотни клинических исследований (КС) ЛС, БАД, ИМН и продуктов питания;
- Имеется свидетельство об аккредитации на право проведения КИ ЛС для медицинского применения всех фаз (I, II, III, IV), а также аккредитацию на право проведения КИ биомедицинских клеточных продуктов;
- КИ ЛС по 30 госпитальным направлениям;
- Проведение КИ в вариантах анализа и оценки доступных данных, испытаний с участием человека и в форме клинико-лабораторных испытаний;
- Наличие локального этического комитета (ЛЭК) по биоэтике;
- Трансфер разработок в практическое здравоохранение: включение в клинические рекомендации и далее — в систему государственного финансирования;
- Регистрация медицинских товаров отечественного и иностранного производства для легального обращения на территории Российской Федерации.
Технологический возможности и парк оборудования НИИ БиоТех








Технологический возможности и парк оборудования НИИ БиоТех
В СамГМУ проводятся доклинические исследования оригинальных и воспроизведенных лекарственных препаратов, физиотерапевтических факторов, изделий медицинского назначения и биомедицинских клеточных продуктов по двухступенчатой системе на клеточных культурах in vitro и на животных in vivo.
Основной площадкой выполнения доклинических исследований является НИИ БиоТех СамГМУ, ответственным специализированным структурным подразделением является Центр доклинических испытаний.
Ключевой задачей Центра доклинических испытаний является проведение доклинических (неклинических) исследований лекарственных средств и медицинских изделий, биомедицинских клеточных продуктов, в том числе изучение токсичности лекарственных средств и БАД, оригинальных и дженериковых, в соответствии с ГОСТ 33044-2014 «Принципы надлежащей лабораторной практики (GLP)».
Оснащение оборудованием для проведения доклинических испытаний позволяет проводить заявленные исследования in vitro и in vivo в полном объеме.
- Автоматическая система мониторинга микроклимата
- Биохимический ветеринарный анализатор
- Гематологический ветеринарный анализатор
- Гистопроцессор скоростной мультифункциональный
- Микротом ротационный
- Станция заливки парафином
- Микроскоп бинокулярный биологический
- Микроскоп медицинский инвертированный
- Ветеринарный наркозно-дыхательный аппарат
- Установка комплексная для содержания лабораторных животных
- Метаболические клетки для животных
- Бокс микробиологической безопасности
- Инкубатор углекислотный медицинский
- Центрифуга высокоскоростная с охлаждением
- Центрифуга медицинская лабораторная
- Морозильная камера низкотемпературная
- Холодильник фармацевтический
- Система для эвтаназии
- Стерилизатор воздушный
- Автоклав
Внутренним партнером Центра доклинических испытаний по вопросам прогнозирования in silico свойств веществ, проведения фармакокинетики и токсикокинетики объектов испытаний является НОЦ «Фармация».
Оснащение оборудованием НОЦ «Фармации» в сфере проведения доклинических испытаний позволяет использовать современный арсенал инструментальных методов анализа для аналитов различной химической структуры.
- Газовый хроматограф с масс-спектрометром
- Газовый хроматограф с пламенно-ионизационным и термоионным детекторами
- Жидкостные хроматографы со спектрофотометрическим и флуориметрическим детекторами
- ИК-спектрометр
- Спектрофлуориметр
- рН-метр
- Стандартное оборудование (весы аналитические, хроматографические камеры, сушильные шкафы и др.)
Возможно совместное выполнение работ и с другими научными и инновационными подразделениями СамГМУ и кафедрами, а также привлечение внешних партнеров (при необходимости).
Значимые публикации в научных отечественных и зарубежных журналах
- Volov, V.T.; Volova, L.T.; Kolsanov, A.V. Information–Thermodynamic Method for the Study of Proliferation of Organized Cellular Structure. Cells 2023, 12, 731. https://doi.org/10.3390/cells12050731
- Astafeva D, Gonda X, Ossina N, Volova L, Sheyfer M, Strelnik A, Lyamin A, Ashurov Z, Syunyakov T, Smirnova D. Peripheral blood mononuclear cell-related biomarkers in schizophrenia // Psychiatria Danubina, 2023; Vol. 35, Suppl. 2, pp 114-122
- Volova, L.T.; Kotelnikov, G.P.; Shishkovsky, I.; Volov, D.B.; Ossina, N.; Ryabov, N.A.; Komyagin, A.V.; Kim, Y.H.; Alekseev, D.G. 3D Bioprinting of Hyaline Articular Cartilage: Biopolymers, Hydrogels, and Bioinks. Polymers 2023, 15, 2695. https://doi.org/10.3390/polym15122695
- Milyudin, E.; Volova, L.T.; Kuchuk, K.E.; Timchenko, E.V.; Timchenko, P.E. Amniotic Membrane Biopolymer for Regenerative Medicine. Polymers 2023, 15, 1213. https://doi.org/10.3390/polym15051213
- Tsiklin, I.L.; Pugachev, E.I.; Kolsanov, A.V.; Timchenko, E.V.; Boltovskaya, V.V.; Timchenko, P.E.; Volova, L.T. Biopolymer Material from Human Spongiosa for Regenerative Medicine Application. Polymers 2022, 14, 941. https://doi.org/10.3390/polym14050941
- Timchenko, P.E.; Timchenko, E.V.; Dolgushkin, D.A.; Frolov, O.O.; Nikolaenko, A.N.; Volova, L.T.; Ionov, A.Yu. Features of the Spectral Surface Estimation of Titanium Implants for Animals. Photonics Russia, 2023; Vol. 4, pp 326-336. https://10.22184/1993-7296.FRos.2023.17
- OPTICAL ANALYSIS OF IMPLANTS FROM THE DURA MATER 16 Timchenko P.E., Timchenko E.V., Frolov O.O., Kiyko N.K., Volova L.T., Nosova M.A., Volov N.V. Optical Memory and Neural Networks. 2018. Т. 27. No 1. С. 46-52. DOI: 10.3103/S1060992X18010101
- Nosova M.A., Sharov A.N., Nefedova I.F., Volova L.T., Trunin D.A. Determination of histological composition at the locus of installation of allogeneic dura mater implant an in vivo model. Laborator-histomorfological research. Tashkent Medical Academy Journals №8,2022, рр. 80-88. DOI: 10.13140/RG.2.2.26220.85128
Доклинические (неклинические) исследования
Доклинические исследования являются обязательным этапом изучения безопасности новой лекарственной субстанции, вещества и их смесей, лекарственных препаратов и БАД, дженериков, биомедицинских клеточных продуктов, в том числе гибридных, медицинских изделий.
Результаты испытаний являются основой для проведения в дальнейшем клинических испытаний, в т.ч. на мощной клинической базе СамГМУ:
На этапе доклинического исследования возможно определить показания и противопоказания к применению лекарственного препарата и других испытуемых объектов, возможные побочные эффекты, установить возможность проведения в дальнейшем клинических испытаний.
В частности, в результате доклинического исследования веществ определяют токсичность и наличие специфической фармакологической активности, дозозависимость эффектов, максимально возможную безопасную дозу, а также целесообразность ее повышения.
Выполнение доклинического исследования завершается формированием подробного заключительного отчета, содержащего информацию обо всех важных аспектах проведенной работы, в том числе информацию об использованных животных/клеточных культурах, способах введения/применения объекта испытания, применяемых концентрациях/уровне воздействия, методиках и оборудовании, а также обработанные данные полученных результатов.
Доклиническое исследование веществ может быть выполнено в целях определения токсичности, фармакодинамики и фармакокинетики объекта изучения, его побочных эффектов, в том числе отдаленных, на тест-системах:
- на клеточных культурах in vitro (изучение безопасности, цитотоксичности, определение цитокинов и др.).
- на животных in vivo (определение класса токсичности вещества, определение общей токсичности, канцерогенности, репродуктивной токсичности, фармакокинетики, фармакодинамики).
Доклиническое исследование медицинских изделий (in vitro и in vivo) включает испытания на биосовместимость и интеграцию тестируемого объекта и тест-системы.
Исследования на клеточных культурах (in vitro)
Проводятся доклинические исследования с использованием первичных культур клеток человека и животных.
На сегодняшний день выполняются исследования на клеточных культурах человека различных линий мезенхимальных стромальных клеток, стромальных клеток, дермальных фибробластов, хондробластов, эпителиоцитов и гемопоэтических стволовых клеток.
- Мезенхимальные стромальные клетки (МСК) - из костного мозга, жировой ткани, пульпы молочных зубов, пуповины.
- Стромальные клетки – из стромы лимфатических узлов.
- Дермальные фибробласты - из кожи взрослого донора (2 источника), из крайней плоти мальчиков, из слизистой десны.
- Хондробласты - из утильных фрагментов дополнительных пальцев детей с полидактилией, из фрагментов ненагруженных участков хрящевой ткани суставов взрослых доноров (гиалиновый хрящ):
- реберного хряща,
- суставного хряща,
- перегородки носа,
- крыльев носа.
- Эпителиоциты - из роговицы, из слизистой десны, из конъюнктивы.
- Гемопоэтические стволовые клетки из костного мозга.
Используется широкая линейка клеточных линий животных:
- МСК костного мозга крыс/кроликов.
- Стромальные клетки из лимфатических узлов крыс.
- Ювенильные дермальные фибробласты новорожденных крыс (спинка, лапки).
- Хондробласты - из мечевидного отростка взрослой крысы, из хрящевой ткани из хвостиков новорожденных крыс (ювенильные клетки), из хрящевой ткани коленного сустава взрослого кролика, из реберного хряща взрослого кролика, из хрящевой ткани суставов новорожденных кроликов (ювенильные клетки).
Возможно получение аутоклеток как человека, так и животных по согласованию с заказчиком (спонсором).
Методы исследований:
- Культуральные методы
- Морфологические методы
- Иммуноморфологические методы
- Биохимические методы
- Физические методы
- Математические методы
Возможно выполнение научно-исследовательских работ по индивидуальному дизайну исследования заказчика (спонсора).
Направления исследований:
- Изучение жизнеспособности, безопасности, пролиферативного потенциала клеток по индивидуальному дизайну (скрининг, предварительная оценка, определение летальных доз и пр.)
- Оценка адгезивных свойств и адгезии клеток к поверхности конкретного материала.
- Разработка новых биомедицинских клеточных продуктов для регенеративной медицины (повреждения суставов, кожи и др.), в том числе путем биопринтинга.
- Разработка 2D- и 3D-носителей для клеток.
- Тестирование in vitro новых и воспроизведенных лекарственных средств и БАД, диагностических методов воздействия, физических и химических методов влияния на клеточные культуры, медицинских изделий и материалов.
- Разработка алгоритмов получения первичных культур клеток и внедрение новых методик в лабораторную практику.
- Создание банков (мастер банков), персонифицированного банка клеток.
Исследования на мелких и крупных животных (in vivo)
Выполнение доклинических исследований проводится с использованием лабораторных животных (крыс, мышей, кроликов), получаемых из крупных сертифицированных питомников России.
Животные содержатся в виварии, представляющем собой современный комплекс помещений, включающий в себя:
- помещения для содержания животных;
- помещения для проведения манипуляций с животными;
- операционную;
- помещение мойки и стерилизации инвентаря и материалов.
В Центре доклинических испытаний созданы все необходимые условия и технологии (чистые помещения, оборудование, стандартные операционные процедуры и квалифицированный персонал), разработаны стандартные операционные процедуры, позволяющие проводить исследования в соответствии с принципами Надлежащей лабораторной практики (GLP).
Проводимые испытания и методики исследований:
- Определение класса острой токсичности (ГОСТ 32644-2014 Острая пероральная токсичность - метод определения класса острой токсичности);
- Испытания по оценке острой токсичности (32296-2013 Основные требования к проведению испытаний по оценке острой токсичности при внутрижелудочном поступлении методом фиксированной дозы и 34557-2019 Испытания по оценке острой токсичности при внутрижелудочном поступлении. Метод вверх и вниз);
- Определение токсичности при повторном многократном пероральном поступлении (ГОСТ 32641-2014 Определение токсичности при повторном многократном пероральном поступлении вещества на грызунах. 28-дневный тест);
- Изучение хронической токсичности (ГОСТ 32519-2013 Изучение хронической токсичности при внутрижелудочном поступлении);
- Изучение подострой (субхронической) токсичности (ГОСТ 32641-2014 Определение токсичности при повторном многократном пероральном поступлении вещества на грызунах. 28-дневный тест, 32637-2020 Повторное исследование пероральной токсичности на грызунах 90 дней);
- Изучение токсичности в соответствии с Руководством по проведению доклинических исследований лекарственных средств. Под ред. Миронова А.Н., Бунатян Н.Д. и др. М., ЗАО «Гриф и К», 2012;
- Исследование фармакокинетики в соответствии с Руководством по проведению доклинических исследований лекарственных средств. Под ред. Миронова А.Н., Бунатян Н.Д. и др. М., ЗАО «Гриф и К», 2012;
- Исследования специфической фармакологической активности, представляющей интерес для заказчика (спонсора).
Морфологические исследования:
Одним из главных этапов при проведении доклинических исследований является патоморфологическая оценка органов и тканей животных (тест-систем).
На основании данной оценки формируется заключение о безопасности вещества, его мишенях в организме, побочных эффектах.
Также выявляются на тканевом уровне изменения, вызванные испытуемыми материалами и медицинскими изделиями, дается оценка характеру и выраженности влияния.
Лаборатория морфологии оснащена современным автоматизированным оборудованием, позволяющим в короткие сроки реализовать комплекс методик по изготовлению гистологических препаратов и их оценке.
Биохимические исследования:
Изучение хронической токсичности и характера влияния на систему гомеостаза, параметров функциональных систем и органов под воздействием биологически активных веществ, биомедицинских клеточных продуктов, медицинских изделий сопровождается оценкой динамики показателей биологических жидкостей лабораторных животных.
Оснащение и компетенции сотрудников позволяют реализовать весь комплекс методов гематологических, биохимических и другие видов исследований.
Фармакокинетические исследования:
Фармакокинетические исследования используются для оценки абсорбции, распределения, метаболизма и экскреции потенциальных биологически активных соединений и являются обязательной частью программы разработки лекарственных средств.
Фармакокинетические данные необходимы для установления зависимости «концентрация/эффект», которая может быть использована для прогнозирования действия кандидата в лекарственные средства у человека.
Данные испытаний позволяют также оптимизировать выбор лекарственной формы.
Результаты фармакокинетического исследования используются в обосновании схем дозирования разрабатываемого средства, которые в последующем уточняются в клинических исследованиях.
Возможно выполнение поисковых научно-исследовательских работ по индивидуальному дизайну исследования заказчика (спонсора), начиная с прогноза видов биологической и фармакологической активности индивидуальных соединений и их смесей.
Администрация Центра и руководители исследований
|
|
|
|
|
Власов Михаил Юрьевич, заведующий ЦДИ, к.б.н
|
Авдеева Елена Владимировна, главный специалист, заместитель заведующего ЦДИ, д.фарм.н |
Шарафутдинова Анастасия Юрьевна, биолог, руководитель Службы обеспечения качества ЦДИ |
|
|
|
|
|
Нефедова Ирина Феликсовна, главный специалист |
Лаптева Елена Игоревна, главный специалист, к.б.н. |
Кулагина Лариса Николаевна, главный специалист |
Сотрудники, задействованные в проведении доклинических исследований, проходят курсы обучения в ведущих научно-исследовательских учреждениях России по программам повышения квалификации, связанным с методологическими основами организации доклинических исследований в соответствии с принципами надлежащей лабораторной практики (GLP), имеют остепененность выше 50%, публикуются в ведущих отечественных и зарубежных научных журналах.
Оформить заявку на проведение исследований можно здесь
1. Описание объекта исследования?
2. Выберите тип исследования:
-
In vivo с использованием лабораторных животных
-
Изучение безопасности по GLP/ГОСТ
- Изучение хронической токсичности при внутрижелудочном поступлении (ГОСТ 32519-2013).
- Повторное исследование пероральной токсичности на грызунах 90 дней (ГОСТ 32637-2020).
- Изучение подострой (субхронической) токсичности при повторном многократном пероральном поступлении вещества на грызунах. 28-дневный тест (ГОСТ 32641-2014).
- Определение токсичности при повторном многократном пероральном поступлении вещества на грызунах. 28-дневный тест) (ГОСТ 32641-2014).
- Оценка класса острой токсичности при однократном внутрижелудочном введении (ГОСТ 32644-2014).
- Оценка острой токсичности при однократном внутрижелудочном введении методом фиксированной дозы (ГОСТ 32296-2013).
- Изучение безопасности по индивидуальному дизайну (скрининг, предварительная оценка, определение летальных доз и пр.)
-
Изучение фармакокинетики
- Укажите тип исследования?
-
Изучение фармакодинамики
- Укажите интересующий профиль активностй
-
Изучение медицинского изделия или материала
- Укажите изучаемые характеристики (биосовместимость, интеграция, иные свойства)?
- Вид животных: мышь / крыса / кролик
- Возраст
- Пол
- Количество животных
- Инбредные / аутобредные / нелинейные
-
- In vitro на клеточных культурах
- Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 5. Исследования на цитотоксичность: методы in vitro (ГОСТ ISO 10993-5- 2023).
- Биологически активные вещества. Оценка цитотоксичности.
- Изучение жизнеспособности, безопасности, пролиферативного потенциала клеток по индивидуальному дизайну (скрининг, предварительная оценка, определение летальных доз и пр.)
- Оценка адгезивных свойств и адгезии клеток к поверхности конкретного материала.
- Разработка новых биомедицинских клеточных продуктов для регенеративной медицины (повреждения суставов, кожи и др.), в том числе полученных путем биопринтинга.
-
Тестирование in vitro новых лекарственных средств и БАД, диагностических методов воздействия, физических и химических методов влияния на клеточные культуры.
- Вид клеток: клетки человека/ клетки животных
- Клеточные линии (человек / крыса / кролик):
- In silico прогноз биологической и фармакологической активности (совместно с НОЦ Фармация)
- Разработка состава действующих веществ (природного и синтетического происхождения) для фармацевтической разработки, БАД, продуктов функционального питания и иной продукции.
3. Укажите контактные данные для связи и адрес электронной почты для направления.
Коммерческого предложения (в течение 3-х рабочих дней).
Связаться по вопросам выполнения работ, сотрудничества и задать уточняющие вопросы можно представителю НИИ БИОТЕХ - Алексею Николаевичу Шарову +7 964 342 16 12 и по электронной почте: me@sharovalex.ru

















.jpeg)
.jpeg)



